
溴化碘(IBr)的化学性质与卤素单质相似,能跟大多数金属反应生成金属卤化物,能跟水反应,IBr+H2O===HBr+HIO。下列有关叙述中不正确的是
A.IBr是双原子分子
B.IBr与水反应时,它既是氧化剂,又是还原剂
C.在很多化学反应中IBr作氧化剂
D.跟NaOH溶液反应可生成NaBr和NaIO
B
【解析】
试题分析:A.一个IBr分子含有1个碘原子1个溴原子,双原子分子,A正确;B.因IBr中I元素的化合价为+1价,Br为-1价,HBr中Br为-1价,HIO中I为+1价,则IBr+ H2O═HBr+HIO中没有元素化合价的变化,该反应属于非氧化还原反应,IBr与水反应时既不做氧化剂,也不做还原剂,B错误;C.溴化碘的化学性质与卤素单质相似,则IBr中I元素的化合价为+1价,I元素的化合价在反应中能降低,则在很多化学反应中IBr是强氧化剂,C正确;D.由反应IBr+ H2O═HBr+HIO可推知与NaOH反应的化学方程式为IBr+2NaOH=NaBr+NaIO+ H2O,D正确;选B。
考点:考查卤素的性质。


 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源:2014-2015学年江苏省连云港市高三上学期期中化学试卷(解析版) 题型:填空题
(12分)铜在我国有色金属材料的消费中仅次于铝,广泛地应用于电气、机械制造、国防等领域。科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO)。回答下列问题:
(1)Mn2+基态的电子排布式可表示为 。
(2)1mol甲醛(HCHO)中含有的σ键数目为 ;
(3)氯和钾与不同价态的铜可生成两种化合物,这两种化合物都可用于催化乙炔聚合,其阴离子均为无限长链结构(如图),a位置上Cl原子的杂化轨道类型为 。已知其中一种化合物的化学式为KCuCl3,另一种的化学式为 ;

(4)金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应生成铜氨离子Cu(NH3)42+,①反应的离子方应程式为 。
②[Cu(NH3)4] 2+中存在的化学键类型有 (填序号)。
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
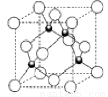
(5)铜的化合物种类也很多,其常见价态为+1、+2价。如CuO、Cu2O、 CuH等。下图是铜的一种氯化物晶体的晶胞结构,则它的化学式是
查看答案和解析>>
科目:高中化学 来源:2014-2015学年重庆复旦中学高一上学期期中化学试卷(解析版) 题型:选择题
下列各组混合物能用分液漏斗直接分离的是
A.柴油与汽油 B.汽油与水 C.溴与水 D.水与乙醇
查看答案和解析>>
科目:高中化学 来源:2014-2015学年重庆复旦中学高二上学期期中化学试卷(解析版) 题型:选择题
在常温下,将等体积的盐酸和氨水混和后,所得溶液的pH=7,则下列说法正确的是
A.原来盐酸的物质的量浓度等于氨水的物质的量浓度
B.所得溶液中c(NH4+)=c(Cl—)
C.所得溶液中c(NH4+)+c(H+)=c(Cl—)
D.所得溶液中c(NH4+)+c(NH3·H2O)=c(Cl—)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年重庆复旦中学高二上学期期中化学试卷(解析版) 题型:选择题
常温下,下列物质的水溶液,其pH值大于7的是
A.KNO3 B.NaHSO4 C.NH4Br D.NaF
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省衢州市五校高一上学期期中化学试卷(解析版) 题型:选择题
下列各反应中,氧化反应与还原反应在同种元素中进行的是
A.Cl2+2NaOH===NaCl+NaClO+H2O
B.2KClO3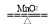 2KCl+3O2↑
2KCl+3O2↑
C.2KMnO4 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
D.2H2O 2H2↑+O2↑
2H2↑+O2↑
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省衢州市五校高一上学期期中化学试卷(解析版) 题型:选择题
下列分离物质的方法中,不正确的是
A.利用分馏的方法从石油中分离出汽油和煤油
B.利用分液的方法将水和酒精分离开来
C.利用结晶的方法除去硝酸钾中混有的少量氯化钾
D.利用过滤的方法除去水中的泥沙
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省衢州市五校高二上学期期中化学试卷(解析版) 题型:填空题
某学生设计了一个“黑笔写红字”的趣味实验,如图所示。滤纸先用氯化钠、无色酚酞
的混合液浸湿,接通电源后,用铅笔在滤纸上写字,会出现红色字迹.据此,回答下列问题:
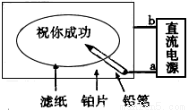
(1)①a端是 极 ②铂片是 极
(2)①铅笔端除了出现红色字迹,还有的现象是 。
②检验铂片的产物的方法是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高一上学期期中化学试卷(解析版) 题型:选择题
对于加热条件下反应3Cl2+6KOH = 5KCl+KClO3+3H2O,以下叙述正确的是
A.Cl2是氧化剂,KOH是还原剂
B.被氧化的Cl原子和被还原的Cl原子的物质的量的比为5∶1
C.Cl2既是氧化剂又是还原剂
D.每生成1mol的KClO3转移6mol的电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com