
| A. | ②④⑥ | B. | ①⑤⑥ | C. | ②③④ | D. | ①⑤⑥⑦ |
分析 ①非金属性越强,氢化物的热稳定性越大;
②He最外层含有2个电子,He为0族元素;
③ⅡA族元素的阳离子比同周期稀有气体元素的原子少一个电子层;
④过渡元素都是金属元素;
⑤核外电子中,离核较近的区域内运动的电子能量较低;
⑥Cl元素的化合价越高,对应的氧化物的水化物的酸性越强;
⑦氯化铝为共价化合物,不存在离子键.
解答 解:①非金属性:F>O>S,则氢化物的热稳定性:HF>H2O>H2S,故①错误;
②最外层两个电子的元素,不一定在第IIA族,如He元素,故②正确;
③ⅡA族元素的阳离子比同周期稀有气体元素的原子少一个电子层,与上一周期稀有气体元素的原子具有相同的核外电子排布,故③正确;
④从ⅢB族到ⅡB族10个纵行的元素都是过渡元素,都是金属元素,故④正确;
⑤核外电子中,离核较近的区域内运动的电子能量较低,离核较远的区域内运动的电子能量较高,故⑤错误;
⑥Cl元素的化合价越高,对应的氧化物的水化物的酸性越强,则酸性:HClO4>HClO3>HClO2>HClO,故⑥错误;
⑦两个非金属元素原子间只可能形成共价键,但是含金属元素的化合物中不一定含离子键,如氯化铝为共价化合物,不含离子键,故⑦错误;
故选D.
点评 本题考查原子结构与元素周期律的关系,题目难度中等,明确元素周期律内容为解答关键,注意掌握原子结构与元素周期律、元素周期表的关系,⑦为易错点,注意氯化铝为共价化合物,试题培养了学生的灵活应用能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
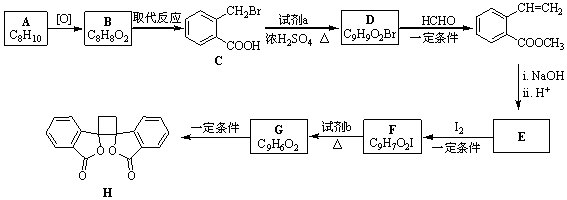
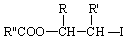
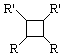
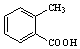 .
.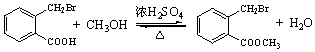 .
. ;此反应同时生成另外一个有机副产物且与F互为同分异构体,此有机副产物的结构简式是
;此反应同时生成另外一个有机副产物且与F互为同分异构体,此有机副产物的结构简式是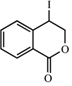 .
.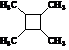 路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件).
路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D |
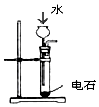 |  | 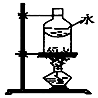 | 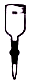 |
| 制乙炔的发生装置 | 蒸馏时的接收装置 | 分离固体氯化钠和碘单质 | 准确量取一定体积K2Cr2O7标准溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
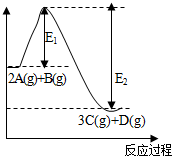 反应2A(g)+B(g)?3C(g)+D(g),△H=akJ/mol.反应过程中的能量变化如图所示.回答下列问题:
反应2A(g)+B(g)?3C(g)+D(g),△H=akJ/mol.反应过程中的能量变化如图所示.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
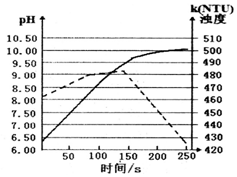 将打磨后的镁条放入盛有50mL蒸馏水的烧杯中,用pH传感器和浊度传感器监测溶液中pH和溶液浊度随时间的变化如图.下列有关描述正确的( )
将打磨后的镁条放入盛有50mL蒸馏水的烧杯中,用pH传感器和浊度传感器监测溶液中pH和溶液浊度随时间的变化如图.下列有关描述正确的( )| A. | 该实验是在常温下进行的 | |
| B. | 实线表示溶液浊度随时间的变化 | |
| C. | 50s时向溶液中滴入酚酞试液,溶液变红 | |
| D. | 150s后溶液浊度下降是因为生成的Mg(OH)2沉降 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烯酸甲酯和甲醇 | B. | 对硝基甲苯和含硝酸的水层 | ||
| C. | 硝酸钾和氯化钠 | D. | 氯化铵和碳酸铵 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知25℃时NH4CN溶液显碱性,则25℃时的电离常数K(NH3•H2O)>K(HCN) | |
| B. | 室温时,相同体积、相同pH的盐酸和醋酸溶液中由水电离出的c(H+):盐酸小于醋酸溶液 | |
| C. | 已知Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12,向含有Cl-、CrO2-4且浓度均为0.010 mol•L-1溶液中逐滴加入0.010 mol•L-1的AgNO3溶液时,CrO2-4先产生沉淀 | |
| D. | 常温下pH=7的CH3COOH和NaOH混合溶液中,c(Na+)>c(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 容器 | 温度(K) | 起始浓度(mol/L) | CH3OH的平衡浓度(mol/L) | ||
| H2 | CO | CH3OH | |||
| ① | 400 | 0.20 | 0.10 | 0 | 0.08 |
| ② | 400 | 0.40 | 0.20 | 0 | x |
| ③ | 500 | 0 | 0 | 0.10 | 0.025 |
| A. | 该反应的正反应是吸热反应 | |
| B. | X=0.16 | |
| C. | 平衡时,容器②中H2的体积分数比容器①的大 | |
| D. | 400K时若再向容器①中充入0.10molH2、0.10molCO和0.10molCH3OH,则平衡将向正反应方向移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com