
下列NaOH溶液中,物质的量浓度为0.1mol/L的是
A.1L溶液中含有4g NaOH B.1L水中溶解4g NaOH
C.1L溶液中含有1g NaOH D.1g溶液中含有0.1mol NaOH
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
 2Cl2+2H2O.5分钟后反应达到平衡,将容器中的混合气体通过过量NaOH溶液,消耗NaOH 2.0mol;再将剩余气体干燥后通过焦性没食子酸的碱性溶液吸收O2,溶液增重19.2g.
2Cl2+2H2O.5分钟后反应达到平衡,将容器中的混合气体通过过量NaOH溶液,消耗NaOH 2.0mol;再将剩余气体干燥后通过焦性没食子酸的碱性溶液吸收O2,溶液增重19.2g.查看答案和解析>>
科目:高中化学 来源: 题型:
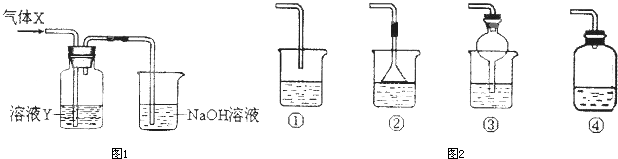
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaOH、AlCl3、盐酸、Na2CO3 | B、BaCl2、AgNO3、Na2CO3、CaCl2 | C、淀粉、淀粉和KI、KI、溴水 | D、NaHCO3、稀硫酸、Na2SiO3、Na2SO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com