
| A、1:1 | B、3:2 |
| C、15:4 | D、5:2 |
科目:高中化学 来源: 题型:
| A、1×10-5mol/L |
| B、1×10-7mol/L |
| C、1×10-9mol/L |
| D、1×10-14mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、废电池、易拉罐 |
| B、废铜烂铁、塑料袋 |
| C、旧报纸、硬纸板 |
| D、包装塑料、啤酒瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25℃时水的电离常数是1.0×10-14 | ||
B、中性溶液的c(H+)=
| ||
| C、纯水在100℃时,c(H+)>10-7mol?L-1,所以此时纯水中c(H+)>c(OH-) | ||
| D、pH<7的溶液一定是酸性溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该反应中反应物总能量高于生成物的总能量 |
| B、该反应只能在较高温度下才能自发进行 |
| C、汽车尾气中的这两种气体均会与人体血红蛋白结合而使人中毒 |
| D、该反应在较低温度下能自发进行,高温和催化剂条件只是加快反应的速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
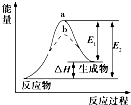
| A、催化剂能降低反应的活化能 |
| B、催化剂能改变反应的焓变 |
| C、该反应的反应热△H=E1-E2 |
| D、a、b分别对应有催化剂和无催化剂的能量变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、Cl-离子的结构示意图: |
| B、HClO的结构式:H-O-Cl |
| C、丙烯的结构简式CH3CH2CH2 |
D、CCl4分子的球棍模型: |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com