
���� ��1�������Ȼ�ѧ����ʽ���ø�˹���ɼ��㷴Ӧ�Ȳ���д�Ȼ�ѧ����ʽ��
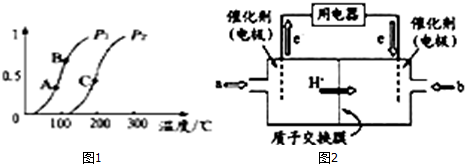
��2������200��ʱ������ͬѹǿ��CO��ת���ʴ�С����ϻ�ѧ����ʽ�з�Ӧǰ�����������仯�������Ӧ���ȣ����¶����ߣ�ƽ�������ƶ�����ѧƽ�ⳣ��K����
�ڿ��淴Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȸ����Ũ�ȱ��ֲ��䣻
��3������ͼ֪������Ĥ�����ӽ���Ĥ����������Һ�����ԣ������������ƶ�����֪��ͨ��a�ĵ缫Ϊ������ͨ��b�ĵ缫Ϊ�����������ϼ״�ʧȥ���ӷ���������Ӧ���������������õ����ӷ�����ԭ��Ӧ��������Һ������ˮ��
��� �⣺��1�����ݸ�˹���ɣ�����֪��Ӧ[��-��-�ۡ�4]��2�õ�CH3OH��l��+O2��g��=CO��g��+2H2O��l�������Ը÷�Ӧ�ġ�H=[��-1274.0kJ/mol��-��-566.0kJ/mol��-��-44.0kJ/mol����4]��2=442kJ•mol-1����CH3OH��l��+O2��g��=CO��g��+2H2O��l����H=-442kJ•mol-1��
�ʴ�Ϊ��CH3OH��l��+O2��g��=CO��g��+2H2O��l����H=-442kJ•mol-1��
��2������ͼa��200��λ�ã�ƽ�������ửһ�����ߣ��ɼ�CH4��ת����P1��P2����CH4��g��+H2O��g��?CO��g��+3H2��g����Ӧ�У������������������ڷ�Ӧ�ѹǿ����ʱƽ���������ƶ�����P1��P2������Ӧ���ȣ����¶����ߣ�ƽ�������ƶ�����ѧƽ�ⳣ��K��������KA��KB��KC��
�ʴ�Ϊ������KA��KB��KC��
�ڿ��淴Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȸ����Ũ�ȱ��ֲ��䣬
a����Ӧǰ�����������ͬ������������ѹǿ�㶨ʱ��Ӧ�ﵽƽ��״̬����a��ȷ��
b������������䣬�����������䣬���������������ܶ�ʼ�պ㶨����b����
c��3v����CH4��=v�棨H2����˵�����淴Ӧ������ȣ���Ӧ�ﵽƽ��״̬����c��ȷ��
d����λʱ��������0.1molCH4ͬʱ����0.3molH2����������Ӧ���ʣ�����˵����Ӧ�ﵽƽ��״̬����d����
�ʴ�Ϊ��ac��
��3������ͼ֪������Ĥ�����ӽ���Ĥ����������Һ�����ԣ������������ƶ�����֪��ͨ��a�ĵ缫Ϊ������ͨ��b�ĵ缫Ϊ�����������ϼ״�ʧȥ���ӷ���������Ӧ��������ӦʽΪ CH3OH-6e-+H2O=CO2+6H+�������������õ��ӷ�����ԭ��Ӧ���缫��ӦʽΪO2+4e-+4H+=2H2O��
�ʴ�Ϊ������O2+4e-+4H+=2H2O��
���� ���⺭���Ȼ�ѧ���绯ѧ�������ݣ���Ҫ��Ӱ�컯ѧƽ�����ء���ѧƽ�ⳣ���ĺ����Ӱ�����ط������漰�缫�ж���缫��Ӧʽ��д�����⣬����ʱע���������ԭ�ĽǶ��ж�ԭ��ص��������Լ��缫����ʽ����д������ԭ���ǹؼ�����Ŀ�Ѷ��еȣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
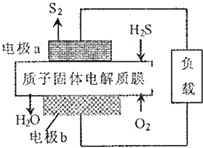 H2S�����ǻ�������õ�������Ӧԭ��Ϊ��2H2S��g��+02��g���TS2��s��+2H20��1����H=-632kJ•mol-1����ͼΪ����ĤH2Sȼ�ϵ��ʾ��ͼ������˵����ȷ���ǣ�������
H2S�����ǻ�������õ�������Ӧԭ��Ϊ��2H2S��g��+02��g���TS2��s��+2H20��1����H=-632kJ•mol-1����ͼΪ����ĤH2Sȼ�ϵ��ʾ��ͼ������˵����ȷ���ǣ�������| A�� | �õ�ؿ�ʵ�ְѻ�ѧ��ȫ��ת��Ϊ���� | |
| B�� | �缫b�Ϸ����ĵ缫��ӦΪ��02+2H2O+4e-�T40H- | |
| C�� | �缫a�Ϸ����ĵ缫��ӦΪ��2H2S-4e-�TS2+4H+ | |
| D�� | ����34gH2S���뷴Ӧʱ����2mo1H+������Ĥ���˸����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
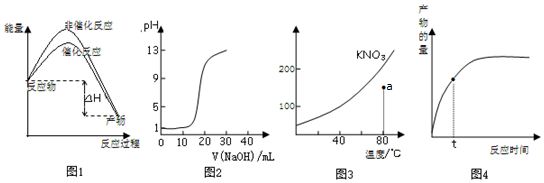
| A�� | ͼ1��ʾ���������Ӱ�췴Ӧ���ʱ� | |
| B�� | ͼ2��ʾ��0.10mol/L CH3COOH��Һ�ζ�20.00 mL0.10mol/LNaOH��Һ���õ��ĵζ����� | |
| C�� | ͼ3��ʾKNO3���ܽ�����ߣ�ͼ�е���ʾ����Һ��80��ʱKNO3�IJ�������Һ | |
| D�� | ͼ4��ʾtʱ����Ӧ���ʴ����淴Ӧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Һ�м�KSCN����Һ�Ժ�ɫ��֤��ԭ��Һ����Fe3+����Fe2+ | |
| B�� | ����ͨ����ˮCuSO4����ĩ������֤��ԭ�����к���ˮ���� | |
| C�� | ���հ�ɫ��ĩ������ʻ�ɫ��֤��ԭ��ĩ����Na+����K+ | |
| D�� | �����ó���ʯ��ˮ������Na2CO3��Һ��NaHCO3��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
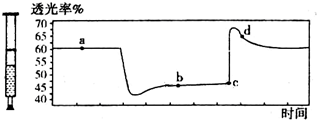 ��֪2NO2�TN2O4+Q ��Q��0������һ������NO2����ע�����к��ڣ���ͼ���������ѹ��ע�����Ĺ���������������ʱ��ı仯��������ɫԽ�����ԽС��������˵����ȷ���ǣ�������
��֪2NO2�TN2O4+Q ��Q��0������һ������NO2����ע�����к��ڣ���ͼ���������ѹ��ע�����Ĺ���������������ʱ��ı仯��������ɫԽ�����ԽС��������˵����ȷ���ǣ�������| A�� | c��IJ���������ע���� | |
| B�� | b����a����ȣ�c��NO2������c��N2O4����С | |
| C�� | ����Ӧ��һ���������н��У���a��b�����ƽ�ⳣ��Ka��Kb | |
| D�� | d�㣺v��������v���棩 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ŵ�ʱ���������Һ��pH���Ͻ���������������PbSO4 ���� | |
| B�� | �ŵ�ʱ��ÿͨ��1mol���ӣ����ؾ�Ҫ����2mol H2SO4 | |
| C�� | ���ʱ��������Ӧ��PbSO4+2e-=Pb+SO42- | |
| D�� | ���ʱ��Ǧ���صĸ�������ӵ�Դ�ĸ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
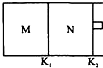 ��ͼ��ʾ������K1�̶�����������K2�������ƶ���T��ʱ��M��N���������о�������ӦN2��g��+3H2��g��?2NH3��g����������M��N�и�����l mol N2��3mol H2����ʼM��N���ݻ����¶���ͬ���������¶Ȳ��䣮����˵���в���ȷ���ǣ�������
��ͼ��ʾ������K1�̶�����������K2�������ƶ���T��ʱ��M��N���������о�������ӦN2��g��+3H2��g��?2NH3��g����������M��N�и�����l mol N2��3mol H2����ʼM��N���ݻ����¶���ͬ���������¶Ȳ��䣮����˵���в���ȷ���ǣ�������| A�� | ��Ӧ�ﵽƽ��ʱN2��ת���ʣ�M��N | B�� | H2�����������M��N | ||
| C�� | NH3��Ũ�ȣ�M��N | D�� | �÷�Ӧ��T��ʱ��ƽ�ⳣ��K��M=N |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Һ����������֮��������㣺c��Na+����c��OH-����c��H+����c��CH3COO-�� | |
| B�� | ����Һ�в������Ӽ����㣺c��CH3COO-��=c��Na+���������Һһ�������� | |
| C�� | ����Һ�����ʽ�ΪCH3COONa�������Ӽ�һ�����㣺c��Na+����c��CH3COO-����c��OH-����c��H+�� | |
| D�� | ����Һ�е�����ΪCH3COONa��CH3COOH������Һ�����Ӽ�������㣺c��CH3COO-����c��Na+����c��H+����c��OH-�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com