
| ������ | ��̿���ڸ��������»�ԭCuO |
| ������ | ��ⷨ����ӦΪ2Cu + H2O  Cu2O + H2���� Cu2O + H2���� |
| ������ | ���£�N2H4����ԭ����Cu(OH)2 |
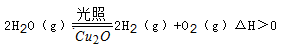
| ��� | �¶� | 0 | 10 | 20 | 30 | 40 | 50 |
| �� | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| �� | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| �� | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
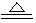 2Cu2O + N2�� + 6H2O
2Cu2O + N2�� + 6H2O  2Cu2O + N2�� + 6H2O
2Cu2O + N2�� + 6H2O 


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
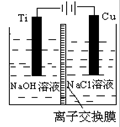
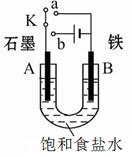
| A����ⱥ��ʳ��ˮ���ռ�������ӽ���Ĥ����������ֹ������ͨ�� |
| B�������϶�пʱ��п�����������ҵ��Һ����п��Ũ���Dz���� |
| C���ö��Ե缫���Na2SO4��Һ������������������ʵ���֮��Ϊ1: 2 |
| D���ö��Ե缫��ⱥ��NaCl��Һ������1 mol����ת�ƣ�������1 molNaOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
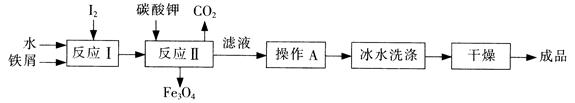

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

A��������ʽ�������ĵ缫��ӦΪ��2H2O��2e�� 2OH�D��H2�� 2OH�D��H2�� |
B���������ң�ͨ�����Һ���ɻ�ɫ��Ϊ��ɫ������Ϊ������H��Ũ������ʹƽ��2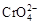 ��2H�� ��2H��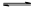 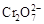 ��H2O�����ƶ� ��H2O�����ƶ� |
C�����Ʊ������ܷ�Ӧ�Ļ�ѧ����ʽΪ��4K2CrO4��4H2O 2K2Cr2O7��4KOH��2H2����2O2�� 2K2Cr2O7��4KOH��2H2����2O2�� |
D���ⶨ����Һ��K��Cr�ĺ�������K��Cr�����ʵ���֮��Ϊd�����ʱ����ص�ת����Ϊ����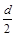 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
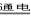 Cu2O+H2��
Cu2O+H2��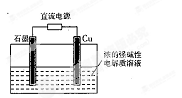
| A��ʯī�缫�ϲ������� |
| B��ͭ�缫�����ĵ缫��ӦΪ��2Cu ��2e��+2OH��= Cu2O+H2O |
| C��ͭ�缫��ֱ����Դ������ |
| D������0��1 mol����ת��ʱ����0��1 molCu2O���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 Al2O3 + 3H2�����������У������ж���ȷ���ǣ�������
Al2O3 + 3H2�����������У������ж���ȷ���ǣ�������| | ԭ��� | ���� |
| A | H+����Pb�缫 | H+����Pb�缫 |
| B | ÿ����3molPb | ����2molAl2O3 |
| C | ������PbO2+4H++2e-=Pb2++2H2O | ������2Al+3H2O-6e-=Al2O3+6H+ |
| D | 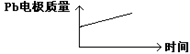 | 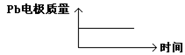 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��NaCl | B��Na2CO3 | C��CuSO4 | D��K2S |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com