
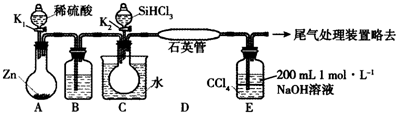
分析 A中Zn和稀硫酸制取氢气,因为SiHCl3能与水发生剧烈反应,所以氢气和SiHCl3反应时需要干燥的氢气,则B装置用浓硫酸干燥氢气,C中SiHCl3变为气态,D中氢气和SiHCl3发生反应生成Si和HCl,用NaOH吸收生成的HCl,然后处理尾气;
(1)水浴加热受热均匀,且产生的气流平稳;
(2)装置D中氢气和SiHCl3发生反应生成Si和HCl;
(3)装置E能吸收生成的HCl,未反应的SiHCl3,还能防倒吸;
(4)先通入氢气,排尽装置中空气,再加热石英管,提高原理利用率,反应完毕停止通氢气;
(5)滴定终点时,氢氧化钠完全反应,溶液红色褪去;
氢氧化钠物质的量等于生成的HCl与后加入HCl的物质的量之和,可以计算生成HCl的物质的量,再根据方程式计算参加反应SiHCl3的质量,进而计算其利用率;
(6)酸能使紫色石蕊试液变红色,氯离子能和硝酸酸化的硝酸银反应生成白色沉淀.
解答 解:A中Zn和稀硫酸制取氢气,因为SiHCl3能与水发生剧烈反应,所以氢气和SiHCl3反应时需要干燥的氢气,则B装置用浓硫酸干燥氢气,C中SiHCl3变为气态,D中氢气和SiHCl3发生反应生成Si和HCl,用NaOH吸收生成的HCl,然后处理尾气;
(1)水浴加热受热均匀,且产生的SiHCl3气流平稳,则D中反应较平稳,故答案为:受热均匀,使产生SiHCl3的气流平稳;
(2)装置D中氢气和SiHCl3发生反应生成Si和HCl,反应方程式为SiHCl3+H2 $\frac{\underline{\;1357K\;}}{\;}$Si+3HCl,
故答案为:SiHCl3+H2 $\frac{\underline{\;1357K\;}}{\;}$Si+3HCl;
(3)装置E中NaOH能吸收生成的HCl,四氯化碳未反应的SiHCl3,还能防倒吸,
故答案为:吸收HCl气体;吸收未反应的SiHCl3;防倒吸;
(4)先通入氢气,排尽装置中空气,再加热石英管,提高原理利用率,反应完毕停止通氢气,②打开K1,装置A中反应一段时间,①加热装置D至1357K:;⑤加热装置C,打开K2,滴加6.5mLSiHC13;④关闭K2;③关闭K1,其合理顺序为:②①⑤④③,
故答案为:②①⑤④③;
(5)滴定终点时,氢氧化钠完全反应,溶液红色褪去,且半分钟不变色;
氢氧化钠物质的量等于生成的HCl与后加入HCl的物质的量之和,则生成HCl的物质的量=0.2L×1mol/L-0.02L×0.1mol/L×$\frac{200mL}{20mL}$=0.18mol,由SiHCl3+H2 $\frac{\underline{\;1357K\;}}{\;}$Si+3HCl,可知参加反应SiHCl3为 $\frac{0.18mol}{3}$=0.06mol,故SiHCl3的利用率为 $\frac{0.06mol×135.5g/mol}{6.5mL×1.34g/mL}$×100%=93.34%,
故答案为:溶液红色褪去,且半分钟不变色;93.34;
(6)酸能使紫色石蕊试液变红色,氯离子能和硝酸酸化的硝酸银反应生成白色沉淀,则检验盐酸的方法为:取两份溶液,一份加入石蕊试液,变红色,说明含有氢离子;另一份加入硝酸酸化的硝酸银溶液,出现白色沉淀,则证明含有氯离子,由此可以鉴定含有盐酸,
故答案为:
取两份溶液,一份加入石蕊试液,变红色,说明含有氢离子;另一份加入硝酸酸化的硝酸银溶液,出现白色沉淀,则证明含有氯离子,由此可以鉴定含有盐酸.
点评 本题考查物质制备,为高频考点,侧重考查学生物质制备、实验操作、物质检验等知识点,明确实验原理、实验操作先后顺序、元素化合物性质是解本题关键,注意题干信息的正确获取和灵活运用,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 向AgI中加一定浓度、一定体积的NaCl溶液,AgI可转化为AgCl | |
| B. | 常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度应该大于$\frac{1}{\sqrt{1.8}}$×10-11mol/L | |
| C. | AgI比AgCl更难溶于水,AgCl可以转化为AgI | |
| D. | 向c(Ag+)=1.8×10-4mol/L的溶液中加入等体积NaCl溶液,开始出现AgCl沉淀,则NaCl溶液浓度应大于1.0×10-6mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
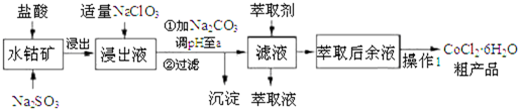
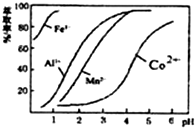
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知酸性高锰酸钾溶液是常用的强氧化剂,可以和草酸钠、二氧化硫等还原性物质发生氧化还原反应.
已知酸性高锰酸钾溶液是常用的强氧化剂,可以和草酸钠、二氧化硫等还原性物质发生氧化还原反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

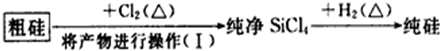
| 物质 | Si | SiCl4 |
| 沸点/℃ | 2355 | 57.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
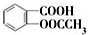 )是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128℃~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐为主要原料合成阿司匹林,反应原理如下:
)是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128℃~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐为主要原料合成阿司匹林,反应原理如下: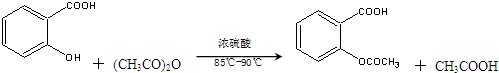
| 名称 | 相对分子质量 | 熔点或沸点(℃) | 水溶性 |
| 水杨酸 | 138 | 158(熔点) | 微溶 |
| 醋酸酐 | 102 | 139.4(沸点) | 易水解 |
| 乙酰水杨酸 | 180 | 135(熔点) | 微溶 |
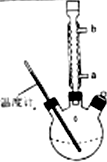
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
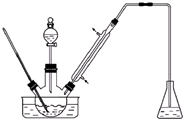 实验室以苯甲醛为原料制备间溴苯甲醛(实验装置见图,相关物质的物理性质见附表).
实验室以苯甲醛为原料制备间溴苯甲醛(实验装置见图,相关物质的物理性质见附表).| 相对分 子质量 | 密度 /(g•cm-3) | 沸点/℃ | |
| 溴 | 160 | 3.119 | 58.8 |
| 苯甲醛 | 106 | 1.04 | 179 |
| 1,2-二氯乙烷 | 99 | 1.2351 | 83.5 |
| 间溴苯甲醛 | 185 | 1.587 | 229 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知X、Y元素同周期,且电负性X>Y,则第一电离能X大于Y | |
| B. | 分子中键能越大,键长越短,则分子越稳定,熔沸点越高 | |
| C. | N-H键键能的含义是拆开约6.02×1023个N-H键所吸收的能量 | |
| D. | H2O中每个O原子结合2个H原子的根本原因是共价键具有方向性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com