
分析 根据混合气体的平均相对分子质量为25及n=$\frac{m}{M}$计算出该混合烃的总物质的量;根据平均相对分子质量可以确定混合气体中一定有甲烷,该混合气通过Br2水时,Br2水增重8.4g,8.4g为烯烃的质量,所以甲烷的质量为1.6g,物质的量为:$\frac{1.6g}{16g/mol}$=0.1mol,从而得出该烯烃的物质的量,结合烯烃的质量和物质的量来确定烯烃的摩尔质量,再根据烯烃组成通式确定烯烃的分子式.
解答 解:混合气体的平均相对分子质量为25,总质量为10g,则该混合烃的物质的量为:$\frac{10g}{25g/mol}$=0.4mol,烯烃的最小相对分子质量为28,烷烃中只有甲烷的相对分子质量小于25,故混合气体中一定有甲烷,该混合气通过Br2水时,Br2水增重的8.4g为烯烃的质量,则甲烷的质量为:10g-8.4g=1.6g,甲烷的物质的量为:$\frac{1.6g}{16g/mol}$=0.1mol,烯烃的物质的量为:0.4mol-0.1mol=0.3mol,M(烯烃)=$\frac{8.4g}{0.3g/mol}$=28g•mol-1,设烯烃的组成为CnH2n,则14n=28,所以n=2,故该烯烃为乙烯,所以混合物为CH4、C2H4;
故答案为:CH4、0.1mol.
点评 本题考查了有机物分子式的确定,题目难度中等,明确乙烯的化学性质为解答关键,注意掌握质量守恒定律在确定有机物分子式中的应用,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | ②⑥⑦ | B. | ②⑤⑦ | C. | ①②⑤⑥⑦ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸盐与盐酸之间的反应 | B. | 一切碳酸盐与一切酸之间的反应 | ||
| C. | 可溶性碳酸盐与强酸之间的反应 | D. | 可溶性碳酸盐与一切酸之间的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 达到化学平衡时,5v正(O2)=4v逆(NO) | |
| B. | 若单位时间内生成x mol NO,同时消耗x mol NH3,则可确定反应达到平衡状态 | |
| C. | 达到化学平衡时,若增大容器的体积,则正反应速率减小,逆反应速率也减小 | |
| D. | 化学反应速率的关系是2v正(NH3)=3v正(H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 肯定不含I- | B. | 可能含有Cu2+ | C. | 一定含有SO32- | D. | 肯定不含有NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 多余的氯气可以用氢氧化钠溶液吸收 | |
| B. | 用澄清的石灰石可以鉴别CO2和SO2 | |
| C. | SO2、Cl2都能使品红溶液褪色,其原理不同 | |
| D. | 铁丝在氯气中燃烧生成三价铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
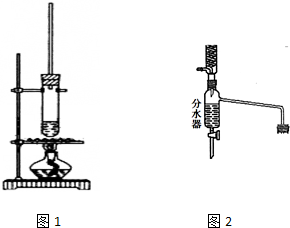 乙酸正丁酯常用作香精,实验室用冰醋酸和正丁醇制备乙酸正丁酯
乙酸正丁酯常用作香精,实验室用冰醋酸和正丁醇制备乙酸正丁酯| 物质 | 密度/g•cm-3 | 沸点/℃ | 溶解度/100g水 |
| 正丁醇 | 0.810 | 118.0 | 9 |
| 冰醋酸 | 1.049 | 118.1 | 互溶 |
| 乙酸正丁酯 | 0.882 | 126.1 | 0.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
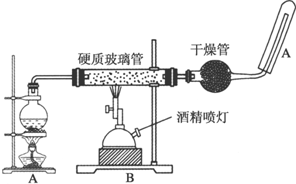
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
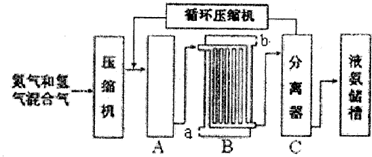
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com