
 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源:华侨中学2006-2007学年高三化学第四次统考试题 题型:013
|
同主族的X、Y、Z三种元素,已知其最高价氧化物对应水化物的酸性强弱是HnXO4<HnYO4<HnZO4,下列推断正确的是 | |
| [ ] | |
A. |
同浓度水溶液的pH值:NanXO4<NanYO4<NanZO4 |
B. |
气态氢化物的稳定性:H8-nX>H8-nX>H8-nZ |
C. |
元素的非金属性:X>Y>Z |
D. |
原子半径:X>Y>Z |
查看答案和解析>>
科目:高中化学 来源:2015届山西省高一下学期期中考试化学试卷(解析版) 题型:填空题
已知A、B、C、X、Y、Z、W为短周期的七种元素,且原子序数依次增大。A的原子半径最小,B是形成化合物种类最多的元素,C元素最外层电子数是次外层电子数的3倍,Z和C同主族;X、Y、W三元素原子的最外层共有11个电子,且三元素的最高价氧化物对应水化物之间两两皆能反应,均能生成盐和水。请回答下列问题:
(1)写出Z元素的原子结构示意图_________________,该元素位于周期表的第______周期,___________族;
(2)写出BC2的电子式____________________,W最高价氧化物对应水化物的化学式___________________________;
(3)写出BC2和X2C2反应的化学方程式_______________________________________;
(4)写出X、Y元素的最高价氧化物对应水化物之间相互反应的离子方程式____________
________________________________________________;
(5)化合物BA4的空间结构是________________________
写出BA4在空气中完全燃烧的化学方程式____________________________________
(6)周期表中与W上下相邻的同族元素形成的气态氢化物中,沸点最高的是 ,(填氢化物化学式),原因是 ;
查看答案和解析>>
科目:高中化学 来源:2014届南京师大附中高一下学期期末调研化学试卷(解析版) 题型:选择题
短周期主族元素X、Y、Z、W,原子序数依次增大。X、Z同主族,X、Y、Z三种元素原子的最外层电子数之和为15,Y原子最外层电子数等于X原子最外层电子数的一半。下列叙述正确的是
A. 非金属性: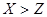
B. 原子半径: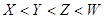
C. 最高价氧化物对应水化物的酸性: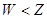
D. 单质Y常温下能溶于浓硝酸
查看答案和解析>>
科目:高中化学 来源:2011-2012学年南京师大附中高一下学期期末调研化学试卷(带解析) 题型:单选题
短周期主族元素X、Y、Z、W,原子序数依次增大。X、Z同主族,X、Y、Z三种元素原子的最外层电子数之和为15,Y原子最外层电子数等于X原子最外层电子数的一半。下列叙述正确的是
A.非金属性: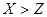 |
B.原子半径: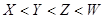 |
C.最高价氧化物对应水化物的酸性: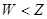 |
| D.单质Y常温下能溶于浓硝酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com