过度排放CO
2会造成“温室效应”,为了减少煤燃烧对环境造成的污染,煤的汽化是高效、清洁利用煤炭的重要途径.煤综合利用的一种途径如图甲所示.
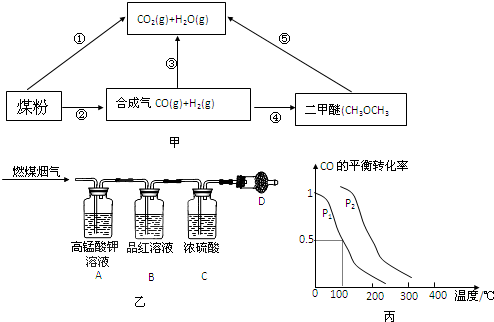
(1)用图乙所示装置定量检测过程①产生的CO
2(提示:煤粉燃烧过程中也会产生SO
2;不考虑空气中的CO
2和水蒸气对检测的影响),B中预期的现象是
,D中的试剂是
(2)已知C(s)+H
2O(g)═CO(g)+H
2(g)△H
1=+131.3kJ/mol
C(s)+2H
2O(g)═CO
2(g)+2H
2(g)△H
2=+90kJ/mol,则一氧化碳与水蒸气反应生成二氧化碳和氢气的热化学方程式是
(3)在容积为VL的密闭容器中充入a mol CO与2a mol H
2,在催化剂作用下反应生成甲醇:CO(g)+2H
2(g)═CH
3OH(g),CO的平衡转化率与温度、压强的关系如图丙所示,则:
①P
1
P
2(填“>”、“<”、或“=”).
②在其它条件不变的情况下,向容器中增加a mol CO与2a mol H
2,达到新平衡时,CO的转化率
(填“增大”、“减小”或“不变”,下同),平衡常数
.
③在P
1下,100℃时,CH
3OH(g)═CO(g)+2H
2(g),反应的平衡常数为
(用含a、V的代数式表示)




 口算能手系列答案
口算能手系列答案