
| A£® | 9ÖÖ | B£® | 8ÖÖ | C£® | 7ÖÖ | D£® | 6ÖÖ |
·ÖĪö ½«Ä³ĢžŌŚŃõĘųÖŠĶźČ«Č¼ÉÕŗó£¬ŅĄ“ĪĶعż×ćĮæµÄÅØH2SO4ŗĶ¼īŹÆ»Ņ£¬ÅØH2SO4ŗĶ¼īŹÆ»Ņ·Ö±šŌöÖŲ10.8gŗĶ22g£¬Ė®µÄĪļÖŹµÄĮæn£ØH2O£©=$\frac{10.8g}{18g/mol}$=0.6mol£¬¶žŃõ»ÆĢ¼ĪļÖŹµÄĮæn£ØCO2£©=$\frac{22g}{44g/mol}$=0.5mol£¬ŌņĢž·Ö×ÓŹ½ĪŖ£ŗC£ŗH=0.5£ŗ0.6”Į2=5£ŗ12£¬·Ö×ÓŹ½ĪŖ£ŗC5H12£¬ĪŖĶéĢž¾Ż“Ė·ÖĪöøĆĢžĖłÓŠĶ¬·ÖŅģ¹¹ĢåµÄŅ»ĀČČ”“śĪļ£®
½ā“š ½ā£ŗ½«Ä³ĢžŌŚŃõĘųÖŠĶźČ«Č¼ÉÕŗó£¬ŅĄ“ĪĶعż×ćĮæµÄÅØH2SO4ŗĶ¼īŹÆ»Ņ£¬ÅØH2SO4ŗĶ¼īŹÆ»Ņ·Ö±šŌöÖŲ10.8gŗĶ22g£¬Ė®µÄĪļÖŹµÄĮæn£ØH2O£©=$\frac{10.8g}{18g/mol}$=0.6mol£¬¶žŃõ»ÆĢ¼ĪļÖŹµÄĮæn£ØCO2£©=$\frac{22g}{44g/mol}$=0.5mol£¬ŌņĢž·Ö×ÓŹ½ĪŖ£ŗC£ŗH=0.5£ŗ0.6”Į2=5£ŗ12£¬·Ö×ÓŹ½ĪŖ£ŗC5H12£¬Ķ¬·ÖŅģ¹¹ĢåÓŠÕżĪģĶ锢ŅģĪģĶ锢ŠĀĪģĶ飬Ņ»ĀČČ”“śĪļ·Ö±šÓŠ3ÖÖ”¢4ÖÖ”¢1ÖÖ£¬¹²ÓŠ8ÖÖ£¬¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éĮĖÓŠ»śĪļ·Ö×ÓŹ½µÄ¼ĘĖćČ·¶Ø”¢Ķ¬·ÖŅģ¹¹ĢåŹéŠ“·½·Ø£¬ÕĘĪÕ»ł“”ŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | KCl | B£® | Na2SO4 | C£® | FeCl3 | D£® | BaCl2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
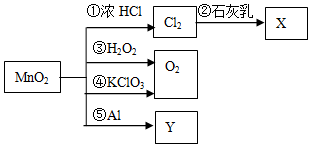
| A£® | ·“Ó¦¢ŁÖŠŃõ»Æ¼ĮÓė»¹Ō¼ĮµÄĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ4 | |
| B£® | ĄūÓĆ·“Ó¦¢ŚæÉÖĘĘÆ°×·Ū£¬·“Ó¦¢ŻæÉÖĘ½šŹōMn | |
| C£® | Éś³ÉµČÖŹĮæµÄO2£¬·“Ó¦¢ŪŗĶ¢Ü×ŖŅʵĵē×ÓŹżĻąµČ | |
| D£® | ŌŚ·“Ó¦¢Ł¢Ū¢Ü¢ŻÖŠ£¬MnO2¾ł×÷Ńõ»Æ¼Į |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆČóŹŖµÄpHŹŌÖ½²āĻ”ĖįČÜŅŗµÄpH£¬²ā¶ØֵʫŠ” | |
| B£® | ²ā¶ØÖŠŗĶ·“Ó¦µÄ·“Ó¦ČČŹ±£¬½«¼ī»ŗĀżµ¹ČėĖįÖŠ£¬Ėł²āĪĀ¶Čֵʫ“ó | |
| C£® | µĪ¶ØĒ°µĪ¶Ø¹ÜÄŚÓŠĘųÅŻ£¬ÖÕµć¶ĮŹżŹ±ĪŽĘųÅŻ£¬Ėł²āĢå»żĘ«Š” | |
| D£® | ÓĆČŻĮæĘæÅäÖĘČÜŅŗ£¬¶ØČŻŹ±ø©ŹÓæĢ¶ČĻߣ¬ĖłÅäČÜŅŗÅضČĘ«“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
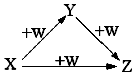 X”¢Y”¢Z”¢WÓŠČēĶ¼ĖłŹ¾µÄ×Ŗ»Æ¹ŲĻµ£Ø·“Ó¦Ģõ¼žŗĶ²æ·ÖĘäĖü·“Ó¦ĪļŹ”ĀŌ£©£¬ŌņX”¢Y”¢ZæÉÄÜŹĒ £Ø””””£©
X”¢Y”¢Z”¢WÓŠČēĶ¼ĖłŹ¾µÄ×Ŗ»Æ¹ŲĻµ£Ø·“Ó¦Ģõ¼žŗĶ²æ·ÖĘäĖü·“Ó¦ĪļŹ”ĀŌ£©£¬ŌņX”¢Y”¢ZæÉÄÜŹĒ £Ø””””£©| A£® | ¢Ł¢Ś¢Ü | B£® | ¢Ś¢Ü | C£® | ¢Ł¢Ś¢Ū | D£® | ¢Ł¢Ś¢Ū¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
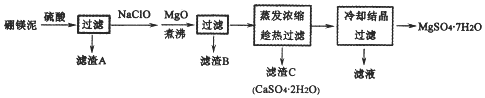
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NH4+”¢Ca2+”¢OH-”¢HCO3- | B£® | NH4+”¢Br-”¢Na+”¢SO42- | ||
| C£® | Ag+”¢H+”¢SO32-”¢ClO- | D£® | H+”¢Cl-”¢Fe2+”¢CO32- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | Ö½Õŵē¼«ŹĒøƵē³ŲµÄÕż¼« | |
| B£® | ļ®²µē¼«·¢ÉśµÄµē¼«·“Ó¦£ŗLi-e-ØTLi+ | |
| C£® | µē³Ų¹¤×÷Ź±£¬µē×Ó“Óļ®²µē¼«¾µ¼ĻßĮ÷ĻņÖ½Õŵē¼«£¬ŌŁ“ÓÖ½Õŵē¼«¾µē½āÖŹČÜŅŗĮ÷Ļņļ®²µē¼« | |
| D£® | øƵē³Ų¾ßÓŠĒįŠĶ”¢ČįŠŌĒŅæÉÕŪµžµÄĢŲµć£¬ÓŠĶūÓ¦ÓĆÓŚČįŠŌµē×ÓĘ÷¼ž |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ĒāŃõ»Æ±µČÜŅŗÓėĮņĖįČÜŅŗ·“Ó¦£ŗBa2++SO42-ØTBaSO4”ż | |
| B£® | ĻņNaAlO2ČÜŅŗÖŠĶØČė¹żĮ涞Ńõ»ÆĢ¼£ŗAlO2-+H2O+CO2ØTAl£ØOH£©3”ż+HCO3- | |
| C£® | ĀČĘųĶØČėĖ®ÖŠ£ŗCl2+H2O?2H++Cl-+ClO- | |
| D£® | NH4ClČÜŅŗŗĶĻ”NaOHČÜŅŗ·“Ó¦£ŗNH4++OH-ØTNH3•H2O |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com