
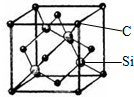
 铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料.请回答:
铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料.请回答:分析 (1)根据元素符号,判断元素原子的核外电子数,再根据核外电子排布规律来写;Cu+的核外有28个电子,根据构造原理书写其基态离子核外电子排布式,原子轨道处于全空、半满或全满时最稳定;
(2)硒、硅均能与氢元素形成气态氢化物分别为H2Se,SiH4,其分子结构分别与H2O,CH4相似;若“Si-H”中键合电子偏向氢原子,说明硅显正价,氢气与硒反应时单质硒是氧化剂,硒显负价;
(3)根据分子晶体的熔、沸点低;根据价层电子对互斥理论确定杂化类型;
(4)根据价层电子对互斥理论确定其杂化方式,提供空轨道的原子和提供孤电子对的原子之间形成配位键;
(5)根据原子晶体的硬度大;每个碳原子连接4个硅原子,每个硅原子又连接其它3个碳原子,据此判断每个C原子周围最近的C原子数目;该晶胞中C原子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,Si原子个数为4,根据ρ=$\frac{m}{V}$计算其密度.
解答 解:(1)Cu元素为29号元素,原子核外有29个电子,所以核外电子排布式为:1s22s22p63s23p63d104s1;CuO中铜的价层电子排布为3d94s0(1分),Cu2O中铜的价层电子排布为3d10,3d10为稳定结构,所以在高温时,能生成Cu2O;
故答案为:1s22s22p63s23p63d104s1;CuO中铜的价层电子排布为3d9,Cu2O中铜的价层电子排布为3d10,后者处于稳定的全充满状态而前者不是;
(2)硒、硅均能与氢元素形成气态氢化物分别为H2Se,SiH4,其分子结构分别V形,正四面体;若“Si-H”中键合电子偏向氢原子,说明硅显正价,氢气与硒反应时单质硒是氧化剂,硒显负价,所以硒与硅的电负性相对大小为Se>Si;
故答案为:V形,正四面体;>;
(3)SeO2常温下白色晶体,熔、沸点低,为分子晶体;二氧化硒分子中价层电子对=2+$\frac{1}{2}$(6-2×2)=3,Se原子的杂化类型为sp2,且含有一个孤电子对,所以属于V形;
故答案为:分子晶体;sp2;
(4)BF3•NH3中B原子含有3个σ 键和1个配位键,所以其价层电子数是4,B原子采取sp3杂化,该化合物中,B原子提供空轨道的原子、N原子提供孤电子对,所以B、N原子之间形成配位键;
故答案为:sp3;配位;
(5)金刚砂(SiC)的硬度为9.5,属于原子晶体;每个碳原子连接4个硅原子,每个硅原子又连接其它3个碳原子,所以每个碳原子周围最近的碳原子数目为3×4=12;该晶胞中C原子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,Si原子个数为4,晶胞边长=a×10-10cm,体积V=(a×10-10cm)3,ρ=$\frac{m}{V}$=$\frac{\frac{40×4}{{N}_{A}}}{(a×1{0}^{-10})^{3}}$g•cm3=$\frac{1.6×1{0}^{32}}{{N}_{A}}$g•cm3;
故答案为:原子晶体;12;$\frac{1.6×1{0}^{32}}{{N}_{A}}$.
点评 本题考查物质结构和性质,涉及晶胞计算、原子杂化判断、原子核外电子排布式的书写等知识点,难点是晶胞计算,题目难度较大.


科目:高中化学 来源: 题型:选择题
| A | B | C | D |
带玻璃塞的试剂瓶 | 聚乙烯盒 | 铁罐车 | 铝制饭盒 |
| 可用于盛放氢氧化钠溶液 | 可用于盛装食品 | 可用于运输浓硫酸 | 不宜长时间存放酸性或碱性的食物 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 时间/min | 0 | 10 | 20 | 40 | 50 | |
| T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | … | 0.15 |
| A. | T2时,NO2的平衡转化率为70.0% | |
| B. | 该反应的△H>0、T1<T2 | |
| C. | 保持其他条件不变,T1时向平衡体系中再充入0.30molCH4和0.80molH2O(g),平衡向正反应方向移动 | |
| D. | 保持其他条件不变,T1时向平衡体系中再充入0.50molCH4和1.20molNO2,与原平衡相比,达新平衡时N2的浓度增大、体积分数减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AlCl3与过量NaOH溶液反应生成AlO${\;}_{2}^{-}$,则与过量NH3•H2O也生成AlO${\;}_{2}^{-}$ | |
| B. | Na2O2与CO2反应生成Na2CO3和O2,则与SO2反应可生成Na2SO3和O2 | |
| C. | Fe与Cl2反应生成FeCl3,则与I2反应可生成FeI3 | |
| D. | Al与Fe2O3能发生铝热反应,则与MnO2也能发生铝热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
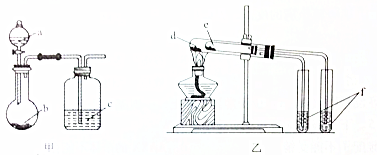
| 选项 | 实验试剂 | 实验结论 | ||
| A | a.稀硫酸 | b.碳酸氢钠 | c.硅酸钠溶液 | 酸性:硫酸>碳酸>硅酸 |
| B | a.稀盐酸 | b.二氧化锰 | c.溴化钠溶液 | 氧化性:MnO2>Cl2>Br2 |
| C | d.小苏打 | e.苏打 | f.石灰水 | 热稳定性:苏打>小苏打 |
| D | d.氯化钠 | e.氯化铵 | f.硝酸银溶液 | 沸点:氯化钠>氯化铵 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上10月月考化学试卷(解析版) 题型:实验题
掌握仪器的名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置.
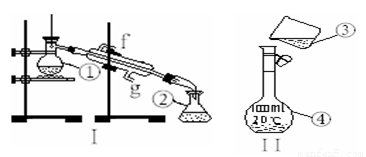
(1)写 出下列仪器的名称:① ②
出下列仪器的名称:① ②
(2)仪器①~④中,使用时必须检查是否漏水的有 .(填序号)
(3)若利用装置I分离丙三醇(能跟水、酒精以任意比互溶,沸点290℃)和酒精(沸点78.2℃)的混合物,还缺少的仪器有 ,将仪器补充完整后进行的实验操作的名称为; .进水方向是 (填g或f),还需加入少量碎瓷片,其作用是  .
.
(4)如图所示装置Ⅱ是转移操作,请指出该操作错误之处:
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市高一上9月调研化学试卷(解析版) 题型:填空题
①容量瓶 ②蒸馏烧瓶 ③量筒 ④烧杯 ⑤分液漏斗 ⑥托盘天平
(1)加热时必须垫石棉网的有:_______________,
(2)使用时必须检查是否漏水的有:________________,
(3)标有温度的有:_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com