
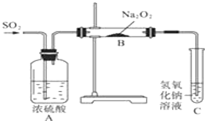
 有两个实验小组探究Na2O2与SO2的反应,都用如图所示装置进行实验.
有两个实验小组探究Na2O2与SO2的反应,都用如图所示装置进行实验.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
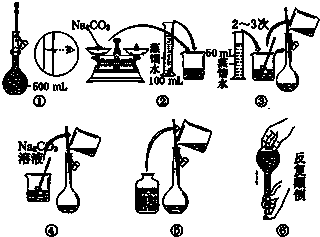 (1)若某药品质量约为32g
(1)若某药品质量约为32g| 50g | 20g | 20g | 10g | 5g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、MnO2 CuO FeO |
| B、(NH4)2SO4 K2SO4 NH4Cl |
| C、AgNO3 KNO3 Na2CO3 |
| D、Na2CO3 CaCO3 K2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、5.8 | B、11.6 |
| C、23.2 | D、46.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+ Na+ SO42- Cl- |
| B、K+ Na+ S2- NO3- |
| C、Mg2+ NH4+ SO42- Cl- |
| D、K+ Na+ AlO2- ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、进行蒸发操作时,当有大量晶体析出,就应停止加热 |
| B、进行蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| C、进行分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D、进行萃取操作时,应选择有机萃取剂,如可用酒精萃取溴水中的溴 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com