
·ÖĪö £Ø1£©ÖŹ×ÓŹżĻąĶ¬£¬ÖŠ×ÓŹż²»Ķ¬µÄŌ×Ó»„³ĘĶ¬Ī»ĖŲ£»
£Ø2£©Ķ¬ÖÖŌŖĖŲŠĪ³ÉµÄ²»Ķ¬µ„ÖŹ»„ĪŖĶ¬ĖŲŅģŠĪĢ壻
£Ø3£©H2”¢D2”¢T2 ¶¼ŹĒĒāŌŖĖŲ×é³ÉµÄ£¬½į¹¹ĻąĶ¬£¬ŹōÓŚĶ¬Ņ»ĪļÖŹ£¬ĪļĄķŠŌÖŹ²»Ķ¬£¬»ÆѧŠŌÖŹĻąĶ¬£»
£Ø4£©ĄūÓĆÅÅĮŠ×éŗĻÅŠ¶ĻČżŌ×Ó»ÆŗĻĪļÖÖĄą£¬“Ó¶ųČ·¶ØĻą¶Ō·Ö×ÓÖŹĮ森
½ā“š ½ā£ŗ£Ø1£©${\;}_{8}^{16}$O”¢${\;}_{8}^{17}$O”¢${\;}_{8}^{18}$OµÄÖŹ×ÓŹżĻąĶ¬£¬ÖŠ×ÓŹż²»Ķ¬£¬»„³ĘĶ¬Ī»ĖŲ£»
${\;}_{1}^{1}$H”¢${\;}_{1}^{2}$H”¢${\;}_{1}^{3}$HµÄÖŹ×ÓŹżĻąĶ¬£¬ÖŠ×ÓŹż²»Ķ¬£¬»„³ĘĶ¬Ī»ĖŲ£»
¹Ź“š°øĪŖ£ŗ¢Ł¢Ü£»
£Ø2£©ŹÆÄ«”¢½šøÕŹÆ¶¼ŹĒÓÉĢ¼ŌŖĖŲŠĪ³ÉµÄ²»Ķ¬µ„ÖŹ£¬»„ĪŖĶ¬ĖŲŅģŠĪĢ壻
¹Ź“š°øĪŖ£ŗ¢Ū£»
£Ø3£©H2”¢D2”¢T2 ¶¼ŹĒĒāŌŖĖŲ×é³ÉµÄ£¬½į¹¹ĻąĶ¬£¬ŹōÓŚĶ¬Ņ»ĪļÖŹ£¬ĪļĄķŠŌÖŹ²»Ķ¬£¬ČēĆÜ¶Č²»Ķ¬£¬»ÆѧŠŌÖŹĻąĶ¬£»
¹Ź“š°øĪŖ£ŗ²»Ķ¬£»ĻąĶ¬£»
£Ø4£©“ÓĒāµÄČżÖÖĶ¬Ī»ĖŲÖŠŃ”Į½øöĒāŌ×Ó£¬Į½øöĒāŌ×ÓæÉŅŌĻąĶ¬Ņ²æɲ»Ķ¬£¬ĖłŅŌĻą¶Ō·Ö×ÓÖŹĮæµÄŗĶ·Ö±šĪŖ2”¢3”¢4”¢5”¢6£»ŃõŌ×ÓĻą¶Ō·Ö×ÓÖŹĮæ·Ö±šĪŖ16”¢17”¢18£¬ĖłŅŌĻą¶Ō·Ö×ÓÖŹĮæµÄÖÖĄąŹżĪŖ7ÖÖ£ŗ18”¢19”¢20”¢21”¢22”¢23”¢24£¬ĘäÖŠ×īŠ”µÄŅ»ÖÖĦ¶ūÖŹĮæŹĒ18g/mol£»
¹Ź“š°øĪŖ£ŗ7£»18g/mol£®
µćĘĄ ±¾Ģāæ¼²éĶ¬Ī»ĖŲ”¢Ķ¬ĖŲŅģŠĪĢ唢Ķ¬Ņ»ĪļÖŹµÄĒų±š£¬ÄŃ¶Č²»“ó£¬×¢Ņā°ŃĪÕøÅÄīµÄÄŚŗÓėĶāŃÓ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ōĒ»łµÄµē×ÓŹ½£ŗ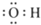 | B£® | Č©»łµÄ½į¹¹¼ņŹ½-COH | ||
| C£® | ŅŅĻ©·Ö×ÓµÄ×ī¼ņŹ½£ŗCH2 | D£® | 1£¬2-¶žäåŅŅĶéµÄ½į¹¹¼ņŹ½£ŗC2H4Br2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
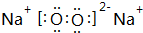 £¬ÓƵē×ÓŹ½±ķŹ¾øĆ»ÆŗĻĪļµÄŠĪ³É¹ż³Ģ
£¬ÓƵē×ÓŹ½±ķŹ¾øĆ»ÆŗĻĪļµÄŠĪ³É¹ż³Ģ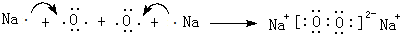 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻņCH3CH2BrÖŠµĪČėAgNO3ČÜŅŗŅŌ¼ģŃéäåŌŖĖŲ | |
| B£® | ¼ģŃéijĀ±“śĢžÖŠŹĒ·ńŗ¬äå£ŗ¼ÓČėNaOHČÜŅŗ£¬¼ÓČČ£¬ĄäČ“£¬ŌŁ¼ÓČėĻõĖįŅųČÜŅŗ | |
| C£® | ±½²»ÄÜÓėäåĖ®·¢ÉśČ”“ś·“Ó¦£¬ÓƱ½ÄÜŻĶČ”äåµÄĖÄĀČ»ÆĢ¼ČÜŅŗÖŠµÄäå | |
| D£® | ĄūÓĆŗĖ“Ź²ÕńĒāĘ×£¬æÉŅŌ¼ų±šCH3OCH3ŗĶCH3CH2OH |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²Ł×÷ | ĻÖĻó |
| ĻņŹ¢ÓŠ4g CaO2µÄ“óŹŌ¹ÜÖŠ¼ÓČė10mLĻ”ŃĪĖįµÄČÜŅŗa | ¾ēĮŅ·“Ó¦£¬²śÉśÄÜŹ¹“ų»šŠĒľĢõø“Č¼µÄĘųĢå |
| Č”5mLČÜŅŗaÓŚŹŌ¹ÜÖŠ£¬µĪČėĮ½µĪŹÆČļ | ČÜŅŗ±äŗģ£¬Ņ»¶ĪŹ±¼äŗóČÜŅŗŃÕÉ«Ć÷ĻŌ±äĒ³£¬ÉŌŗó£¬ČÜŅŗ±äĪŖĪŽÉ« |

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ć°°×Īķ£¬»ģŗĻĪļĪĀ¶ČÉżøß | B£® | ²śÉś»ĘĀĢÉ«ĘųĢå | ||
| C£® | Ć°°×Īķ£¬»ģŗĻĪļĪĀ¶Č½µµĶ | D£® | ŅŗĢåĖĽ¦£¬Ć°°×ŃĢ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com