
【题目】为探究浓度对化学平衡的影响,某同学进行如下实验:下列说法不正确的是:

A.该实验通过观察颜色变化以判断生成物浓度的变化
B.观察到现象a比现象b中红色更深,即可证明增加反应物浓度,平衡正向移动
C.进行II、III对比实验的主要目的是防止由于溶液体积变化引起各离子浓度变化而干扰实验结论得出
D.若I中加入KSCN溶液的体积改为2mL也可以达到实验目的
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】PCl3和PCl5都是重要的化工原料.将PCl3(g)和Cl2(g)充入体积不变的2L密闭容器中,在一定条件下发生下述反应,并于10min时达到平衡:PCl3(g)+Cl2(g)![]() PCl5(g) △H<0,有关数据如下:
PCl5(g) △H<0,有关数据如下:
PCl3(g) | Cl2(g) | PCl5(g) | |
初始浓度(mol/L) | 2.0 | 1.0 | 0 |
平衡浓度(mol/L) | c1 | c2 | 0.4 |
下列判断不正确的是
A. 10 min内,v(Cl2)=0.04 mol/(Lmin)
B. 当容器中Cl2为1.2 mol时,反应达到平衡
C. 升高温度,反应的平衡常数增大,平衡时PCl3的物质的量浓度<1.6mol/L
D. 平衡后移走2.0 mol PCl3和1.0 molCl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 X、Y、Z、W均为短周期元素,他们在元素周期表的位置如下图所示。若Y原子的最外层电子数与电子总数之比为3:4,下列说法正确的是

A. 原子半径:W>Z>Y>X
B. 最高价氧化物对应水化物的酸性:Z>W>X
C. 气态氢化物的稳定性:Z>W
D. W的单质能与水反应,生成一种具有漂白性的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的![]() 与足量的碳在体积可变的恒压密闭容器中反应:
与足量的碳在体积可变的恒压密闭容器中反应:![]() ,平衡时,体系中气体体积分数与温度的关系如图所示,下列说法正确的是
,平衡时,体系中气体体积分数与温度的关系如图所示,下列说法正确的是
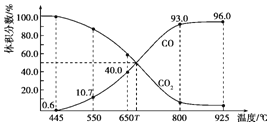
A.![]() 时,若充入惰性气体,
时,若充入惰性气体,![]() 、
、![]() 逆均减小,平衡不移动
逆均减小,平衡不移动
B.![]() 时,反应达平衡后
时,反应达平衡后![]() 的转化率为
的转化率为![]()
C.![]() 时,若充入等体积的
时,若充入等体积的![]() 和CO,平衡向逆反应方向移动
和CO,平衡向逆反应方向移动
D.平衡常数的关系:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可根据烷烃的同分异构体判断卤代烃的种数。步骤如下:
①利用减碳移位法书写出对应烷怪的同分异构体:
②判断各同分异构体中等效氢的数目。判断等效氢的规律为同一碳原子上的氢原子等效;同一碳原子上的甲基氢原子等效;位于对称位置上的碳原子上的氢原子等效。
③用卤素原子取代等效氢原子,有几种不同的氢,其一元取代物就有几种。
分子式为C5H11Cl的同分异构体共有(不考虑立体异构)
A.6种B.7种C.8种D.9种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第三代混合动力车,可以用电动机、内燃机或二者结合推动车辆。汽车上坡或加速时,电动机提供推动力,降低汽油的消耗;在刹车或下坡时,电池处于充电状态,其电路工作原理如图所示。下列说法中正确的是
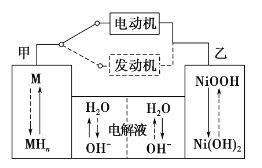
A.放电时甲为负极,充电时为阳极
B.放电时负极的电极反应式为:MHn-ne-=M+nH+
C.电池充电时,OH-由甲侧向乙侧移动
D.汽车下坡时发生图中实线所示的过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取Fe、FeO、Fe2O3的均匀混合物质量为7.2g,向其中加入200 mL 1 mol·L-1的盐酸,恰好使混合物完全溶解,放出1120 mL(标准状况)的气体。所得溶液中,加入KSCN溶液无血红色出现,那么若用足量的CO在高温下还原相同质量的此混合物,能产生铁的质量为 ( )
A. 1.4g B. 2.8g C. 5.6g D. 11.2g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用平衡移动原理解释的是
A. 开启啤酒瓶后,瓶中马上泛起大量泡沫
开启啤酒瓶后,瓶中马上泛起大量泡沫
B. 由H2(g)、I2(g)、HI(g)组成的平衡体系加压后颜色变深
由H2(g)、I2(g)、HI(g)组成的平衡体系加压后颜色变深
C.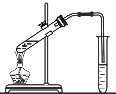 实验室制取乙酸乙酯时,将乙酸乙酯不断蒸出
实验室制取乙酸乙酯时,将乙酸乙酯不断蒸出
D. 石灰岩受地下水长期溶蚀形成溶洞
石灰岩受地下水长期溶蚀形成溶洞
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间(t)产生氢气体积(V)的数据,根据数据绘制如图,则曲线a、b、c、d所对应的实验组别可能是( )

组别 | c(HCl)/(molL-1) | 温度/℃ | 状态 |
1 | 2.0 | 25 | 块状 |
2 | 2.5 | 30 | 块状 |
3 | 2.5 | 50 | 粉末状 |
4 | 2.5 | 30 | 粉末状 |
A.④—③—②—①B.①—②—③—④
C.③—④—②—①D.①—②—④—③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com