
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
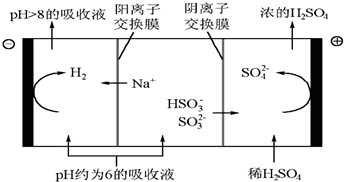
分析 (1)①根据溶液中电荷守恒和物料守恒确定溶液中各种离子浓度的关系;
②阳极上阴离子放电发生氧化反应;
(2)根据混合气体的体积计算混合气体的物质的量,结合气体体积比计算甲烷、氢气的物质的量,再根据热化学反应方程式计算放出的热量.注意燃烧后恢复至常温,氢气燃烧放出的热量应选择生成液态水的热化学反应方程式计算.
解答 解:(1)①当溶液呈中性时,溶液中氢离子浓度等于氢氧根离子浓度,亚硫酸氢根离子浓度大于亚硫酸根离子浓度.
A、溶液呈电中性,溶液中阴阳离子所带电荷相等,溶液呈中性时,溶液中氢离子浓度等于氢氧根离子浓度,所以c(Na+)=2c(SO32-)+c(HSO3-),故A正确.
B、溶液呈中性时,溶液中氢离子浓度等于氢氧根离子浓度,亚硫酸氢根离子浓度大于亚硫酸根离子浓度,溶液中阴阳离子所带电荷相等,所以得c(Na+)>c(HSO3-)>c(SO32-)>c(H-)=c(OH-),故B正确.
C、溶液呈电中性,溶液中阴阳离子所带电荷相等,得c(Na+)+c(H-)=2c(SO32-)+c(HSO3-)+c(OH-),故C错误.
故答案为:AB;
②当吸收液的pH降至约为6时,吸收液中阴离子主要是亚硫酸氢根离子,亚硫酸氢根离子在阳极上失电子和水反应生成硫酸根离子和氢离子,电极反应式为:HSO3-+H2O-2e-=SO42-+3H+.
故答案为:HSO3-+H2O-2e-=SO42-+3H+;
(2)甲烷和氢气的混合气体11.2L(已折合成标准状况),所以甲烷和氢气的混合气体的总的物质的量为$\frac{11.2}{22.4}$=0.5mol,
甲烷和氢气的体积比为4:1,所以甲烷的物质的量为0.5mol×$\frac{4}{5}$=0.4mol,氢气的物质的量为0.5mol-0.4mol=0.1mol.
由CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-Q1kJ/mol可知,
0.4mol甲烷燃烧放出的热量为0.4mol×Q1kJ/mol=0.4Q1kJ;
由2H2(g)+O2(g)═2H2O(l)△H=-Q3kJ/mol可知,
0.1mol氢气燃烧生成液态水放出的热量为0.1mol×$\frac{1}{2}$×Q3kJ/mol=0.05Q3kJ.
所以放出的热量为0.4Q1+0.05Q3,
故答案为:0.4 Q1+0.05Q3.
点评 本题考查了污染物的处理,涉及到离子方程式、化学方程式和离子浓度大小的比较、热化学方程式计算反应热,等知识点,难度中等,需要注意的是比较溶液中各种离子浓度相对大小时要结合电荷守恒和物料守恒分析解答.


科目:高中化学 来源: 题型:多选题
| A. | 新制氯水中:c(H+)=c(HClO)+2c(ClO-)+c(OH-) | |
| B. | pH=8的NaClO2溶液中:c(Na+)>c(ClO2-)>c(OH-)>c(H+) | |
| C. | 0.1mol•L-1HCl溶液与0.2 mol•L-1 NH3•H2O溶液等体积混合pH>7:c(NH3•H2O)>c(Cl-)>c(NH4+)>c(OH-) | |
| D. | 0.1mol•L-1K2C2O4溶液与0.2 mol•L-1KHC2O4溶液等体积混合:4c(K+)=3[c(C2O42-)+c(HC2O4-)] |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 没有阳光 | B. | 温度太低 | C. | 压强太大 | D. | 缺少CO2和O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{4c-b-2a}{2}$ kJ | B. | $\frac{4c+b-2a}{2}$ kJ | C. | (4c+b-2a) kJ | D. | (4c-b+2a) kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
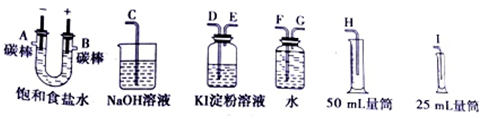
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | α粒子的结构示意图: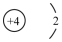 | B. | α粒子就是氦原子的原子核 | ||
| C. | α粒子的核外电子数为2 | D. | α粒子的质量数为2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 37C l与39K的中子数不等 | B. | 12C与14C的质子数相等 | ||
| C. | H3O+与OH-的电子数相等 | D. | 15N2与14N2摩尔质量不等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com