
���� ��1����Ӧ2KNO3+3C+S=K2S+N2��+3CO2���У�N��SԪ�صĻ��ϼ۽��ͣ�CԪ�صĻ��ϼ����ߣ���Ԫ�ػ��ϼ۽��͵�����Ϊ������������������ԭ������Ԫ�ػ��ϼ����ߵ�����Ϊ��ԭ������ԭ������������Ӧ�IJ���Ϊ���������ϻ��ϼ۵ı仯����ת�Ƶ�����Ŀ��
��2���ڼ�������������ͭ���ȷֽ����������ͭ�������������塢���������ݷ�Ӧ�������ͷ�Ӧ����д����Ӧ�ķ�Ӧ����ʽ�����ݻ��������������ռ�ı����Ϳ�����������ռ�ı���������ȷ�����
��� �⣺��1���ڷ�Ӧ2KNO3+3C+S=K2S+N2��+3CO2���У�NԪ�صĻ��ϼ���+5����Ϊ0��SԪ�صĻ��ϼ���0����Ϊ-2�ۣ���KNO3��S����������CԪ�صĻ��ϼ���0���ߵ�+4����C����ԭ��������������Ӧ��CO2Ϊ��������÷�Ӧת��12e-������˫�ŷ��������ת�Ƶķ�����ĿΪ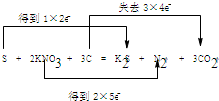 ��
��
�ʴ�Ϊ�� ��KNO3��S��CO2��
��KNO3��S��CO2��
��2���ڼ�������������ͭ���ȷֽ����������ͭ�������������塢��������ѧ����ʽ��2Cu��NO3��2$\frac{\underline{\;\;��\;\;}}{\;}$2CuO+4NO2��+O2�����ɷ���ʽ���ɵIJ����֪������ռ�ı����Ϳ�����������ռ�ı���������ȣ����Ѵ����ǵ�ľ������ֽ�����Ļ�������У�ľ����ȼ����˵��������������ȼ��
�ʴ�Ϊ��2Cu��NO3��2$\frac{\underline{\;\;��\;\;}}{\;}$2CuO+4NO2��+O2�����ܣ����������������ռ�ı����Ϳ�����������ռ�ı���������ȣ����NO2���岻����ȼ����ľ�����Ḵȼ��
���� ���⿼��������ԭ��Ӧ�Լ�����ͭ�ֽ������жϣ�Ϊ��Ƶ���㣬���շ�Ӧ��Ԫ�صĻ��ϼ۱仯Ϊ���Ĺؼ�������������ԭ��Ӧ��������Ŀ��飬ע��˫���ŵķ�������Ŀ�ѶȲ���


 A�ӽ��� ϵ�д�
A�ӽ��� ϵ�д� ȫ�Ų��Ծ�ϵ�д�
ȫ�Ų��Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Zn2+ | B�� | Zn | C�� | Cu | D�� | H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2 | B�� | HCOOH | C�� | C6H12O6 | D�� | C12H22O11 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������õİ뵼����� | |
| B�� | �������Ͻ���۵���������۵㣬Ӳ��С | |
| C�� | ������������������˰��Ļ�ѧ���� | |
| D�� | Ư�ۡ���������������ˮ�ľ�������ԭ������ͬ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��1����֪�ڳ��³�ѹ�£�
��1����֪�ڳ��³�ѹ�£��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 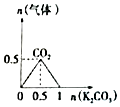 n ��HCl��=1mol��K2CO3���뵽HCl��Һ�У��ڱֿ����������ɵ����� | |
| B�� | 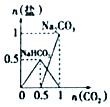 n��NaOH��=1mol��CO2ͨ�뵽NaOH��Һ�з�Ӧ���ɵ��� | |
| C�� | 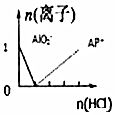 n��NaAlO2��=1mol��HCl���뵽NaAlO2��Һ�����ӵĴ������ | |
| D�� | 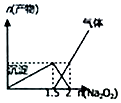 n��AlCl3��=1mol��Na2O2����AlCl3��Һ��Ӧ�IJ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
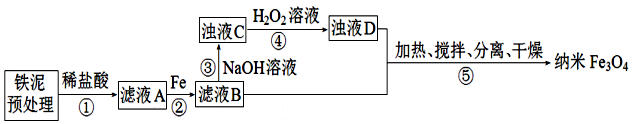
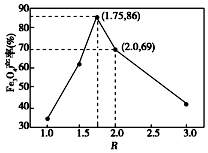
| ������ | Fe��OH��3 | Fe��OH��2 |
| ��ȫ������PH | 3.0 | 8.3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com