

已知碳酸钠的溶解度(S)随温度变化的曲线如下图所示:

回答下列问题:
(1)滤渣的主要成分为________________。
(2)“趁热过滤”的原因是________________________________________。
(3)若在实验室进行“趁热过滤”,可采取的措施是_______________________(写出1种)。
(4)若“母液”循环使用,可能出现的问题及其原因是_____________________________。
(5)已知:Na2CO3·10H2O(s)![]() Na2CO3(s)+10H2O(g) ΔH1=+532.36 kJ·mol-1
Na2CO3(s)+10H2O(g) ΔH1=+532.36 kJ·mol-1
Na2CO3·10H2O(s)![]() Na2CO3·H2O(s)+9H2O(g) ΔH2=+473.63 kJ·mol-1
Na2CO3·H2O(s)+9H2O(g) ΔH2=+473.63 kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式______________________________。
(1)Mg(OH)2、Fe(OH)3、CaCO3
(2)使析出的晶体为Na2CO3·H2O,防止因温度过低而析出Na2CO3·10H2O晶体,令后续的加热脱水耗时长
(3)用已预热的布氏漏斗趁热抽滤
(4)问题:溶解时有大量沉淀生成,使Na2CO3损耗且产物Na2CO3混有杂质;原因:“母液”中,含有的离子有Ca2+、Na+、Cl-、![]() 、OH-,
、OH-,![]() ,当多次循环后,使离子浓度不断增大,溶解时会生成CaSO4、Ca(OH)2、CaCO3等沉淀
,当多次循环后,使离子浓度不断增大,溶解时会生成CaSO4、Ca(OH)2、CaCO3等沉淀
(5)Na2CO3·H2O(s)![]() Na2CO3(s)+H2O(g);ΔH=+58.73 kJ·mol-1
Na2CO3(s)+H2O(g);ΔH=+58.73 kJ·mol-1
解析:(1)因工业碳酸钠中含有Mg2+、Fe3+、Ca2+,所以“除杂”中加入过量的NaOH溶液,可生成Mg(OH)2、Fe(OH)3、CaCO3沉淀。
(2)观察坐标图,温度减少至308 K时发生突变,溶解度迅速减少,若不趁热过滤将析出晶体Na2CO3·7H2O。
(3)思路方向:①减少过滤的时间;②保持过滤时的温度。
(4)思路:分析“母液”中存在的离子,若参与循环,将使离子浓度增大,对工业生产中所得产品的质量有所影响。
(5)通过观察两个热化学方程式,可将两式相减,从而得到Na2CO3·H2O(s)![]() Na2CO3(s)+H2O(g)。
Na2CO3(s)+H2O(g)。


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:
碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料。工业碳酸钠(纯度约98%)中含有Ca2+、Mg2+、Fe3+、Cl-和![]() 等杂质,提纯工艺路线如下:
等杂质,提纯工艺路线如下:

已知碳酸钠的溶解度(S)随温度变化的曲线如下图所示:
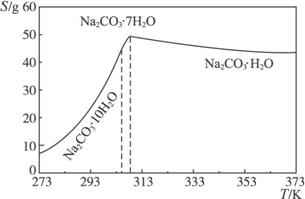
回答下列问题:
(1)滤渣的主要成分为________________。
(2)“趁热过滤”的原因是________________________________________。
(3)若在实验室进行“趁热过滤”,可采取的措施是_______________________(写出1种)。
(4)若“母液”循环使用,可能出现的问题及其原因是_____________________________。
(5)已知:Na2CO3?10H2O(s)![]() Na2CO3(s)+10H2O(g) ΔH1=+532.36 kJ?mol-1
Na2CO3(s)+10H2O(g) ΔH1=+532.36 kJ?mol-1
Na2CO3?10H2O(s)![]() Na2CO3?H2O(s)+9H2O(g) ΔH2=+473.63 kJ?mol-1
Na2CO3?H2O(s)+9H2O(g) ΔH2=+473.63 kJ?mol-1
写出Na2CO3?H2O脱水反应的热化学方程式______________________________。
查看答案和解析>>
科目:高中化学 来源:2008年普通高等学校招生统一考试化学试题(广东卷) 题型:填空题
碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料。工业碳酸钠(纯度约98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO 等杂质,提纯工艺路线如下:
等杂质,提纯工艺路线如下:
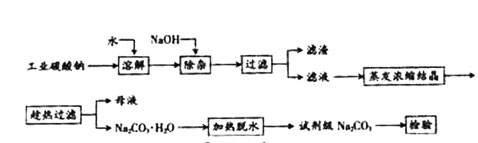
已知碳酸钠的溶解度(S)随温度变化的曲线如下图所示:
回答下列问题:
【小题1】(1)滤渣的主要成分为 。
【小题2】(2)“趁热过滤”的原因是 。
【小题3】(3)若在实验室进行“趁热过滤”,可采取的措施是 (写出1种)。
【小题4】(4)若“母液”循环使用,可能出现的问题及其原因是 。
【小题5】(5)已知:
Na2CO3·10H2O(s)=Na2CO3(s)+10H2O(g) ΔH1=" +532.36" kJ·mol-1
Na2CO3·10H2O(s)=Na2CO3·H2O(s)+9H2O(g) ΔH1=" +473.63" kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2010年江苏省高二第二学期期末考试化学试卷 题型:填空题
(12分)碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料。工业碳酸钠(纯度约98%)中含有Ca2+、Mg2+、Fe3+、Cl—和SO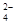 等杂质,提纯工艺路线如下:已知碳酸钠的溶解度(S)随温度变化的曲线如下图所示。
等杂质,提纯工艺路线如下:已知碳酸钠的溶解度(S)随温度变化的曲线如下图所示。

回答下列问题:
(1)滤渣的主要成分为 。
(2)“趁热过滤”的原因是 。
(3)若“母液”循环使用,可能出现的问题及其原因是 。
(4)已知:Na2CO3·10H2O(s)=Na2CO3(s)+10H2O(g) ΔH1=+532.36 kJ·mol-1
Na2CO3·10H2O(s)=Na2CO3·H2O(s)+9H2O(g) ΔH1=+473.63 kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com