
| A. | 氢键比分子间作用力强,所以它属于化学键 | |
| B. | 分子内形成的氢键使物质的熔点和沸点升高 | |
| C. | 氨溶于水后氨分子和水分子之间形成了氢键 | |
| D. | 邻羟基苯甲酸的熔点比对羟基苯甲酸的熔点高 |
分析 A.氢键属于分子间作用力;
B.分子内形成的氢键使物质的熔点和沸点降低;
C.氨溶于水后氨分子和水分子结合生成一水合氨;
D.对羟基苯甲酸易形成分子之间氢键.
解答 解:A.氢键、范德华力均属于分子间作用力,氢气的作用大于范德华力,故A错误;
B.分子内形成的氢键使物质的熔点和沸点降低,分子间形成的氢键使物质的熔点和沸点升高,故B错误;
C.氨溶于水后氨分子和水分子结合生成一水合氨,一水合氨分子与水分子之间存在氢气,故C错误;
D.对羟基苯甲酸易形成分子之间氢键,而邻羟基苯甲酸形成分子内氢键,所以邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低,故D正确.
故选D.
点评 本题考查氢键及氢键对物质的性质的影响,明确氢键主要影响物质的物理性质是解答本题的关键,题目难度不大.


 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:选择题
| A. | NaCN中氮元素的化合价为+3 | |
| B. | 用双氧水处理现场前,应紧急疏散群众 | |
| C. | 每生成1molNH3转移2mol电子 | |
| D. | NaCN中既含有离子键又含有共价键的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3+ Na+ S2- Cl- | B. | Al3+ NH4+ AlO2- NO3- | ||
| C. | NH4+ Mg2+ SO42- Cl- | D. | H+ Na+ HCO3- SiO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
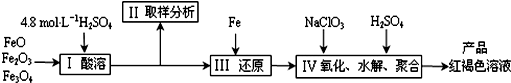
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定浓度的氨水加水稀释的过程中,$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)}$的比值减小 | |
| B. | 浓度均为0.1 mol•L-1的Na2CO3、NaHCO3混合溶液中:[c(CO32-)>c(HCO3-),且2c(Na+)═3c(H2CO3)+3c(HCO3-)+3c(CO32-) | |
| C. | 常温下0.4mol/LHB溶液和0.2mol/LNaOH溶液等体积混合后溶液的pH=3,则溶液中微粒浓度存在下面关系:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-) | |
| D. | 假设HClO的电离平衡常数为Ka,碳酸的电离常数分别记为:Ka1 和Ka2,已知:Ka1>Ka>Ka2,则发生反应:2NaClO+CO2(少量)+H2O═Na2CO3+2HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图为实验室蒸馏自来水得到少量蒸馏水的装置示意图如图2,请根据图示回答下列问题:
如图为实验室蒸馏自来水得到少量蒸馏水的装置示意图如图2,请根据图示回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将40g NaOH固体溶解于1L水中 | |
| B. | 将22.4L氯化氢气体溶于水配成lL溶液 | |
| C. | 将1L 10mol/L的浓盐酸与9L水混合 | |
| D. | 20g NaOH固体溶解在水中配成500mL溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com