
”¾ĢāÄæ”æĻćÄūĆŹÓĶŹĒ“ÓĻćÄūĆŹŹ÷µÄ¹ūʤ֊ĢįĮ¶µÄéŁ×ÓĪ¶µÄĻćÓĶ£¬33%µÄÅ®ÓĆĻćĖ®ÓƵ½ĮĖÕāÖÖŌĮĻ”£ĻćÄūĆŹÓĶŗ¬Ī¢ĮæµÄĻćÄūĆŹ·ÓŗĶĻćÄūĆŹĆŃ£¬Ęä½į¹¹ČēÓŅĶ¼”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ

A. ĻćÄūĆŹĆѵķÖ×ÓŹ½ĪŖC13H6O4
B. ĻćÄūĆŹ·ÓæÉÓė¼×Ėį·“Ó¦×Ŗ»Æ³ÉĻćÄūĆŹĆŃ
C. 1 molĻćÄūĆŹ·Ó×ī¶ąæÉÓė2 mol Br2·¢Éś·“Ó¦
D. 1 molĻćÄūĆŹ·Ó×ī¶ąæÉŅŌÓė3 mol NaOHČÜŅŗ·“Ó¦
”¾“š°ø”æD
”¾½āĪö”æŹŌĢā·ÖĪö£ŗA”¢øł¾ŻÓŠ»śĪļÖŠĢ¼Ō×ÓµÄĢŲµć£¬“ĖÓŠ»śĪļµÄ·Ö×ÓŹ½ĪŖ£ŗC13H8O4£¬¹Ź“ķĪó£»B”¢ŗĶ¼×Ėį·¢Éśõ„»Æ·“Ó¦£¬¶ų²»ŹĒĆŃ£¬¹Ź“ķĪó£»C”¢ŗ¬ÓŠ2øöĢ¼Ģ¼Ė«¼ü£¬1molĻćÄūĆŹĆŃÓė2molBr2·¢Éś¼Ó³É·“Ó¦£¬ōĒ»ł¶ŌĪ»±½»·ÉĻĒāŌ×ÓŗĶäå·¢ÉśČ”“ś·“Ó¦£¬Ņņ“Ė1molĻćÄūĆŹĆŃ×ī¶ąŗĶ3moläåµ„ÖŹ·¢Éś·“Ó¦£¬¹Ź“ķĪó£»D”¢1molĻćÄūĆŹ·Óŗ¬ÓŠ1mol·ÓōĒ»łŗĶ1molõ„µÄ½į¹¹£¬Ņņ“ĖĻūŗÄ2molNaOH£¬Ė®½āŗó×ó¶ĖŗĶ±½»·Ö±½ÓĻąĮ¬µÄO£¬×Ŗ»Æ³É·ÓōĒ»ł£¬ŌŁĻūŗÄ1molĒāŃõ»ÆÄĘ£¬Ņņ“Ė¹²ĻūŗÄ3molNaOHČÜŅŗ£¬¹ŹÕżČ·”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĖę×ÅČĖĆĒÉś»īÖŹĮæµÄ²»¶ĻĢįøߣ¬·Ļµē³Ų±ŲŠė½ųŠŠ¼ÆÖŠ“¦ĄķµÄĪŹĢā±»Ģįµ½ŅéŹĀČÕ³Ģ£¬ĘäŹ×ŅŖŌŅņŹĒ
A£®»ŲŹÕĘäÖŠµÄŹÆÄ«µē¼«
B£®ĄūÓƵē³ŲĶāæĒµÄ½šŹō²ÄĮĻ
C£®·ĄÖ¹µē³ŲÖŠ¹Æ”¢ļÓŗĶĒ¦µČÖŲ½šŹōĄė×Ó¶ŌĶĮČĄŗĶĖ®×ŹŌ“µÄĪŪČ¾
D£®²»Ź¹µē³ŲÖŠÉųŠ¹µÄµē½āÖŹøÆŹ“ĘäĖūĪļĘ·
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄ³ČŻĘ÷ÖŠ·¢ÉśŅ»øö»Æѧ·“Ó¦£¬·“Ó¦¹ż³ĢÖŠ“ęŌŚH2O”¢ClO£”¢CN£”¢HCO3£”¢N2”¢Cl£ĮłÖÖĄė×Ó”£ŌŚ·“Ó¦¹ż³ĢÖŠ²āµĆClO£ŗĶN2µÄĪļÖŹµÄĮæĖꏱ¼ä±ä»ÆµÄĒśĻßČēĶ¼ĖłŹ¾”£ĻĀĮŠÓŠ¹ŲÅŠ¶ĻÖŠ²»ÕżČ·µÄŹĒ

A£®»¹Ō¼ĮŹĒŗ¬CN£µÄĪļÖŹ£¬Ńõ»Æ²śĪļ²»Ö»ÓŠN2
B£®Ńõ»Æ¼ĮŹĒClO££¬»¹Ō²śĪļŹĒHCO3£
C£®²ĪÓė·“Ó¦µÄŃõ»Æ¼ĮÓė»¹Ō¼ĮµÄĪļÖŹµÄĮæÖ®±ČĪŖ5£ŗ2
D£®±ź×¼×“æöĻĀČōÉś³É2.24LN2Ōņ×ŖŅʵē×ÓĪŖ1mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĆčŹöÖŠ£¬²»ÕżČ·µÄŹĒ
A.FeSO4 æÉÓĆÓŚ·ĄÖ¹Ź³Ę·Ńõ»Æ±äÖŹ£¬ŃÓ³¤Ź³Ę·µÄ±£ÖŹĘŚ
B.ĻņFe2£ØSO4£©3 ČÜŅŗÖŠ¼ÓČėŅ»¶ØĮæµÄĶ·Ū£¬Ķ·ŪČ«²æ·“Ó¦ŗó£¬ČÜŅŗÖŠŅ»¶Øŗ¬ÓŠFe2+
C.ĪļÖŹNaHCO3”¢Al2O3”¢Fe2O3”¢Al£ØOH£©3”¢Al ¶¼¼ČÄÜøśŃĪĖį·“Ó¦, ÓÖÄÜøśĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦
D.ĢśŌŚŃõĘųÖŠČ¼ÉÕ£¬Éś³ÉŗŚÉ«µÄFe3O4
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀ±ķŹĒA”¢B”¢C”¢D”¢EĪåÖÖÓŠ»śĪļµÄÓŠ¹ŲŠÅĻ¢£ŗ
A | B | C | D | E |
¢ŁŹĒŅ»ÖÖĢž£¬ÄÜŹ¹äåµÄĖÄĀČ»ÆĢ¼ČÜŅŗĶŹÉ« ¢Ś±ČĄżÄ£ŠĶĪŖ£ŗ
¢ŪÄÜÓėĖ®ŌŚŅ»¶ØĢõ¼žĻĀ·“Ӧɜ³ÉC | ¢ŁÓÉC”¢HĮ½ÖÖŌŖĖŲ×é³É ¢ŚĒņ¹÷Ä£ŠĶĪŖ£ŗ
| ¢ŁÄÜÓėÄĘ·“Ó¦£¬µ«²»ÄÜÓėNaOHČÜŅŗ·“Ó¦£» ¢ŚÄÜÓėE·“Ӧɜ³ÉĻą¶Ō·Ö×ÓÖŹĮæĪŖ100µÄõ„ | ¢ŁÓÉC”¢H”¢BrČżÖÖŌŖĖŲ×é³É£» ¢ŚĻą¶Ō·Ö×ÓÖŹĮæĪŖ109 | ¢ŁÓÉC”¢H”¢OČżÖÖŌŖĖŲ×é³É£» ¢ŚĒņ¹÷Ä£ŠĶĪŖ£ŗ
|
øł¾Ż±ķÖŠŠÅĻ¢»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Š“³öAŹ¹äåµÄĖÄĀČ»ÆĢ¼ČÜŅŗĶŹÉ«µÄ»Æѧ·½³ĢŹ½£ŗ________________________£»
£Ø2£©AÓėĒāĘų·¢Éś¼Ó³É·“Ó¦ŗóÉś³É·Ö×ÓF£¬FµÄĶ¬ĻµĪļµÄĶØŹ½ĪŖCnH2n£«2”£µ±n £½________Ź±£¬ÕāĄąÓŠ»śĪļæŖŹ¼ÓŠĶ¬·ÖŅģ¹¹Ģ唣
£Ø3£©BµÄ·Ö×ÓŹ½ĪŖ________£¬Š“³öŌŚÅØĮņĖį×÷ÓĆĻĀ£¬BÓėÅØĻõĖį·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ___ £»
£Ø4£©D”śAĖł¼ÓŹŌ¼Į¼°·“Ó¦Ģõ¼žĪŖ____________________£»·“Ó¦ĄąŠĶĪŖ__________________£»
£Ø5£©CÓėE·“Ó¦ÄÜÉś³ÉĻą¶Ō·Ö×ÓÖŹĮæĪŖ100µÄõ„£¬Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ_____________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»ĀČ¼×Ķé(CH3C1)ŹĒŅ»ÖÖÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬³£ĪĀĻĀĖüŹĒĪŽÉ«ÓŠ¶¾ĘųĢ壬Ī¢ČÜÓŚĖ®£¬Ņ×ČÜÓŚŅŅ“¼”¢CCl4µČ”£
£Ø1£©¼××éĶ¬Ń§ŌŚŹµŃéŹŅÓĆĻĀĶ¼ĖłŹ¾×°ÖĆÄ£Äā“߻ƷØÖʱøŗĶŹÕ¼ÆŅ»ĀČ¼×Ķ锣
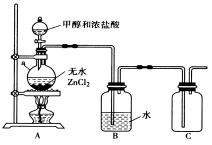
¢Ł ĪŽĖ®ZnCl2ĪŖ“߻ƼĮ£¬aĘæÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ____________________________”£
¢Ś ×°ÖĆBµÄÖ÷ŅŖ×÷ÓĆŹĒ____________________”£
¢ŪŹÕ¼Æµ½µÄCH3ClĘųĢåŌŚŃõĘųÖŠ³ä·ÖČ¼ÉÕ£¬²śĪļÓĆ¹żĮæµÄV1mL”¢c1mol”¤L-1NaOHČÜŅŗ³ä·ÖĪüŹÕ£¬ŅŌ¼×»ł³Č×÷ÖøŹ¾¼Į£¬ÓĆc2 mol”¤L-1ŃĪĖį±ź×¼Ņŗ¶ŌĪüŹÕŅŗ½ųŠŠ·µµĪ¶Ø(·¢ÉśµÄ·“Ó¦ĪŖ£ŗ
NaOH+HCl= NaCl+H2O ,Na2CO3+2HCl£½2NaCl+2CO2”ü+2H2O)£¬×īÖÕĻūŗÄV2 mLŃĪĖį”£ŌņĖłŹÕ¼ÆCH3ClµÄĪļÖŹµÄĮæĪŖ_____ _ mol”£(ŅŃÖŖ£ŗ2CH3Cl+3O2![]() 2CO2+2H2O+2HCl)
2CO2+2H2O+2HCl)
£Ø2£©ŅŅ×éĶ¬Ń§Ń”ÓĆ¼××éA”¢B×°ÖĆŗĶĻĀĶ¼ĖłŹ¾µÄ²æ·Ö×°ÖĆ¼ģŃéCH3ClÖŠµÄĀČŌŖĖŲ”£
(ŅŃÖŖ£ŗŅ»Ā±“śĶéŅ»°ćŅŖŌŚ¼ÓČČĢõ¼žĻĀ²ÅÄÜÓėĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦)
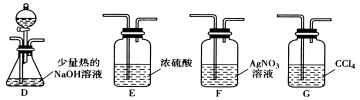
¢ŁŅŅ×éĶ¬Ń§µÄŹµŃé×°ÖĆÖŠ£¬ŅĄ“ĪĮ¬½ÓµÄŗĻĄķĖ³ŠņĪŖA”śB”ś________”ś__ ”ś ”£
¢ŚĶØČėŅ»¶ĪŹ±¼äµÄCH3ClĘųĢ壬“ņæŖ×°ÖĆDÖŠ·ÖŅŗĀ©¶·µÄ»īČū£¬¹Ū²ģŹµŃéĻÖĻ󔣷ÖŅŗĀ©¶·ÖŠŹ¢·ÅµÄŹŌ¼ĮŹĒ_______ŗĶ_________”£
¢ŪÄÜÖ¤Ć÷CH3ClÖŠŗ¬ÓŠĀČŌŖĖŲµÄŹµŃéĻÖĻóŹĒ_____________________________”£
£Ø3£©²éŌÄ׏ĮĻæÉÖŖ£ŗAgNO3µÄŅŅ“¼ČÜŅŗæÉŅŌ¼ģŃéCH3XÖŠµÄĀ±ĖŲŌ×Ó”£Ļą¹ŲŹż¾ŻČēĻĀ±ķ£ŗ

¢ŁCH3XĶØČėAgNO3µÄŅŅ“¼ČÜŅŗÖŠ£¬³żÓŠ³ĮµķÉś³ÉĶā£¬»¹Éś³ÉĻõĖį¼×õ„£¬ĒėŠ“³öĻõĖį¼×õ„µÄ½į¹¹¼ņŹ½£ŗ______________________________”£
¢Ś½«CH3ClŗĶCH3BrµÄ»ģŗĻĘųĢåĶØČėAgNO3µÄŅŅ“¼ČÜŅŗÖŠ£¬ĻČ³öĻÖµ»ĘÉ«³Įµķ”£ĒėŅĄ¾Ż±ķÖŠŹż¾Ż½āŹĶŌŅņ____________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĢ«ŌŹŠ¼ŅÓĆČ¼ĮĻµÄøüŠĀ¾ĄśĮĖŅŌĻĀ¼øøö¹ż³Ģ£ŗ

Ēė»Ų“šĻĀĮŠĪŹĢā”£
£Ø1£©ĪŖĮĖŹ¹Ćŗ³ä·ÖČ¼ÉÕ£¬æɲÉČ”µÄ“ėŹ©ŹĒ ”£
£Ø2£©ĆŗµÄĘų»ÆæɲśÉś¹ÜµĄĆŗĘų£¬ĘäÖ÷ŅŖ·“Ó¦ŹĒĢ¼ÓėĖ®ÕōĘųŌŚøßĪĀĻĀÉś³ÉĮ½ÖÖ³£¼ūµÄæÉČ¼ŠŌĘųĢ壬ÕāĮ½ÖÖĘųĢåŹĒ ”£
£Ø3£©Ņŗ»ÆŹÆÓĶĘųµÄÖ÷ŅŖ³É·ÖŹĒ±ūĶé£ØC3H8£©£¬±ūĶéĶźČ«Č¼ÉյĻÆѧ·“Ó¦·½³ĢŹ½ŹĒ ”£
£Ø4£©ĢģČ»Ęų×÷Č¼ĮĻ±ČĆŗøüĒå½ąµÄŌŅņŹĒ £Ø“šŅ»Ģõ¼“æÉ£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŹµŃ黳±¾²Ł×÷£Ø»ņŹµŃé×¢ŅāŹĀĻī£©ÖŠ£¬Ö÷ŅŖæ¼ĀĒŹµŃé°²Č«µÄŹĒ£Ø £©
A. ŹµŃéŹ£ÓąµÄŅ©Ę·²»ÄÜ·Å»ŲŌŹŌ¼ĮĘæ B. æÉČ¼ŠŌĘųĢåµÄŃé“æ
C. ĘųĢåŹµŃé×°ÖĆŌŚŹµŃéĒ°½ųŠŠĘųĆÜŠŌ¼ģ²é D. µĪ¹Ü²»Äܽ»²ęŹ¹ÓĆ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŖĢ½Ė÷¹¤Ņµŗ¬ĀĮ”¢Ģś”¢ĶŗĻ½š·ĻĮĻµÄŌŁĄūÓĆ£¬»ÆѧæĘ¼¼Š”×éµÄĶ¬Ń§ĆĒ½ųŠŠĮĖŅ»ĻµĮŠŹµŃéĢ½¾æ”£ĖūĆĒÉč¼ĘµÄŹµŃé·½°øČēĶ¼£¬ĘäÖŠYĘųĢåŹĒæÕĘųµÄÖ÷ŅŖ³É·ÖÖ®Ņ»”£

Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©²Ł×÷¢ŁÓƵ½µÄ²£Į§ŅĒĘ÷ÓŠÉÕ±”¢ ”£
£Ø2£©ĘųĢåXµÄ·Ö×ÓŹ½ĪŖ ”£
£Ø3£©·“Ó¦¢ÜµÄ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ ”£
£Ø4£©³£ĪĀĻĀ£¬½«ĀĢ·ÆÅä³ÉŌ¼0.1molL£1FeSO4ČÜŅŗ£¬²āµĆČÜŅŗµÄpH=3”£ĒėÓĆĄė×Ó·½³ĢŹ½½āŹĶŌŅņ £¬øĆČÜŅŗÖŠc(SO42£)£c(Fe2+)= molL£1£ØĢīŹżÖµ£©”£
£Ø5£©ČōŅŖ²ā¶ØĖłÅäČÜŅŗÖŠFe2+µÄ×¼Č·ÅØ¶Č£¬Č”20.00mLČÜŅŗӌ׶ŠĪĘæÖŠ£¬æÉŌŁÖ±½ÓÓĆĖįŠŌKMnO4±ź×¼ČÜŅŗ½ųŠŠµĪ¶Ø£¬µĪ¶ØÖÕµćµÄĻÖĻóŹĒ ”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com