
| A. | E表示生成铜的物质的量 | B. | E表示生成硫酸的物质的量 | ||
| C. | F表示反应消耗水的物质的量 | D. | E表示反应生成氧气的物质的量 |
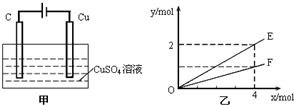
分析 由甲可知,为电解装置,C为阳极,发生4OH--4e-=O2↑+2H2O,Cu为阴极,发生Cu2++2e-=Cu;由乙可知,转移4mol电子生成2molE,E为Cu,生成1molF,F为氧气,以此来解答.
解答 解:由甲可知,为电解装置,C为阳极,发生4OH--4e-=O2↑+2H2O,Cu为阴极,发生Cu2++2e-=Cu,总反应为2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+2H2SO4,结合乙可知,转移4mol电子生成2molE,生成1molF,
A.由电子与物质的物质的量的关系可知,E表示反应生成铜的物质的量,故A正确;
B.因硫酸与和转移电子的物质的量相等,则E能表示生成硫酸的物质的量,故B正确;
C.由总反应可知,Cu与水的物质的量相同,则E表示反应消耗水的物质的量,故C错误;
D.由电子与物质的物质的量的关系可知F表示反应生成氧气的物质的量,故D错误;
故选CD.
点评 本题考查电解原理,明确发生的电极反应、电解反应及图象的分析是解答本题的关键,注意反应中转移电子与各物质的物质的量的关系即可解答,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | Zn | B. | Fe | C. | Mg | D. | Al |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用FeCl3溶液腐蚀铜线路板:Cu+Fe3+═Cu2++Fe2+ | |
| B. | Na2O2与H2O反应产生O2:2Na2O2+2H2O═4Na++4OH-+O2↑ | |
| C. | 将铁溶于稀盐酸:2Fe+6H+═2Fe3++3H2↑ | |
| D. | 向氯化铝溶液中加入过量的氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知甲烷的燃烧热为890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═2CO2(g)+2H2O(g)△H=-890.3 kJ/mol | |
| B. | 已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| C. | 已知中和热为△H=-57.3 kJ/mol,则1mol稀硫酸和足量稀NaOH溶液反应的反应热就是中和热 | |
| D. | 已知S(g)+O2(g)═SO2(g)△H1;S(s)+O2(g)═SO2(g)△H2,则△H1<△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操作 | 现象 | 结论 |
| A | 将浓硫酸滴到胆矾晶体中 | 固体变白 | 浓硫酸有脱水性 |
| B | 常温下将Al片放入浓硫酸中 | 无明显变化 | Al与浓硫酸不反应 |
| C | 向某溶液中加入BaCl2溶液,再向溶液中加入盐酸 | 产生白色沉淀 | 该溶液中含有SO42- |
| D | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置 | 下层溶液显紫红色 | 氧化性:Fe3+>I2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com