
| A.铝片不用特殊方法保存 |
| B.生铁比纯铁易生锈 |
| C.制氢气时用粗锌而不用纯锌 |
| D.工程施工队在铁制水管外刷一层“银粉” |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:实验题
| A.铁片置于硫酸铜溶液中有铜析出; |
| B.铁、铜与氯气反应分别生成FeCl3、CuCl2; |
| C.铜片置于FeCl3溶液中,铜片逐渐溶解(2FeCl3+Cu=2FeCl2+ CuCl2) |
| D.铁片、铜片分别置于盛有稀硫酸的烧杯中,铁片上有气泡产生,而铜片无气泡 |
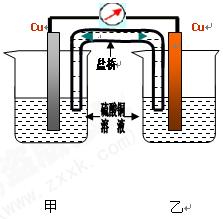
 及电极均相同,两杯溶液的温度不同,可否形成原电池
及电极均相同,两杯溶液的温度不同,可否形成原电池| 甲杯硫酸铜浓度 mol/L | 0.8 | 0.8 | 0.8 | 0.8 | 0.8 | 0.8 |
| 乙杯硫酸铜浓度 mol/L | 0.8 | 0.4 | 0.2 | 0.1 | 0.05 | 0.025 |
| 两杯溶液浓度差值 | 0 | 0.4 | 0.6 | 0.7 | 0.75 | 0.775 |
| 电压 mV | 0 | 6 | 12 | 16 | 22 | 26 |
电流 mA mA | 0 | 0.02 | 0.04 | 0.06 | 0.07 | 0.08 |
| 甲杯硫酸铜温度℃ | 19 | 19 | 19 | 19 | 19 | 19 |
| 乙杯硫酸铜温度℃ | 19 | 29 | 39 | 49 | 59 | 69 |
| 两杯溶液温差℃ | 0 | 10 | 20 | 30 | 40 | 50 |
| 电压 mV | 0 | 6.1 | 12 | 20 | 27 | 34 |
| 电流 mA | 0 | 0.025 | 0.047 | 0.07 | 0.15 | 0.18 |
 面有铜析出。
面有铜析出。
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.镍氢电池、锂离子电池和锌锰干电池都是二次电池 |
| B.燃料电池是一种高效且不会污染环境的新型电池 |
| C.化学电池的反应基础是复分解反应 |
| D.铅蓄电池放电的时候正极是Pb,负极是PbO2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 金属 | 电子流动方向 | 电压/V |
| Fe | Fe → Cu | +0.78 |
| Zn | Zn → Cu | +1.10 |
| A | Cu → A | -0.15 |
| B | B → Cu | +0.3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.钢铁腐蚀时,铁有时候作负极有时候作正极 |
| B.将铜片锌片用导线连接插入稀硫酸中,铜是阳极,铜片上有氢气产生 |
| C.用惰性电极电解氯化铜溶液时氯气在阳极产生 |
| D.电解氯化钠溶液时电子从负极经过溶液流向正极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
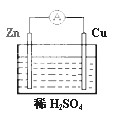
| A. Zn是负极 | B.Cu是正极 |
| C.负极上发生氧化反应 | D.正极上发生氧化反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com