
| 1 |
| 2 |


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:
| A、1升的0.1mol L-lNaHCO3溶液中含有0.1NA个HCO3- |
| B、17g氨气中含有的氢原子数为3NA |
| C、标准状况下,2.24LCCl4中含共价键数为0.4NA |
| D、常温常压下,2.24L甲烷中含有甲烷分子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
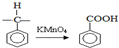
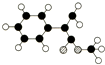 化学-选修有机化学基础
化学-选修有机化学基础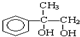 拟从
拟从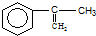 出发合成A.
出发合成A.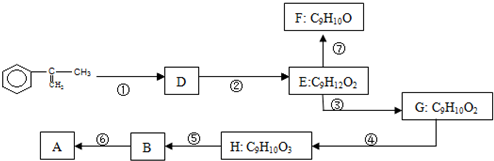
| HBr |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向Fe(NO3)2溶液中滴加稀硫酸 |
| B、将盐酸滴入NaAlO2溶液中 |
| C、向碳酸氢钠溶液中滴加氢氧化钠溶液 |
| D、加热溶有SO2的品红溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 容器代号 | A | B | C | D |
| 平衡时混合物平均式量 | 16 | 17 | ||
| 平衡时N2的转化率 | 20% | |||
| 平衡时H2的转化率 | 30% |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(A-)=c(K+) |
| B、c(H+)=c(OH-)<c(K+)<c(A-) |
| C、V总≥20mL |
| D、V总≤20mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
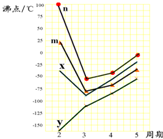
| A | B | C | D | E | F | |
| 主要化合价 | -1 | -3+5 | -2+6 | -1+7 | +2 | +1+2 |
| 原子半径 | 0.071 | 0.11 | 0.102 | 0.099 | 0.197 | 0.117 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com