
【题目】三氟化硼是平面正三角形,因此是非极性分子,推断三氯甲烷(碳原子位于分子结构中心)的结构和分子的极性情况是( )
A. 四面体,极性分子 B. 平面三角形,非极性分子
C. 正四面体,非极性分子 D. 平面三角形,极性分子
 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:
【题目】取一小块钠放在玻璃燃烧匙里加热,下列实验现象正确的是( )
①金属先熔化②在空气中燃烧火焰呈黄色③燃烧时火星四射
④燃烧后生成淡黄色固体⑤燃烧后生成白色固体
A.①②③B.①②④C.①②⑤D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中符合下列图象的是( ) 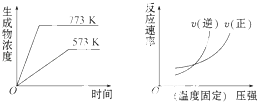
A.N2(g)+3H2(g)2NH5(g)△H=﹣Q1kJmol﹣1(Q1>0)
B.2SO5(g)2SO2(g)+O2(g)△H=+Q2kJmol﹣1(Q2>0)
C.4NH5(g)+5O2(g)4NO(g)+6H2O(g)△H=﹣Q3kJmol﹣1(Q3>0)
D.H2(g)+CO(g)C(g)+H2O(g)△H=+Q4kJmol﹣1(Q4>0)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.95℃纯水的pH<7,说明加热可导致水呈酸性
B.pH=3的醋酸溶液稀释至10倍后pH=4
C.0.2 mol/L的盐酸与0.1 mol/L的盐酸等体积水混合后pH=1.5
D.pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH<7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸、碱、盐均属于电解质,它们的水溶液中存在各种平衡.
(1)氨水是中学常见的碱溶液 ①下列事实可证明NH3H2O是弱碱的是(填字母序号).
A.常温下,0.1molL﹣1氨水pH为11
B.氨水能跟氯化亚铁溶液反应生成氢氧化亚铁
C.常温下,0.1molL﹣1氯化铵溶液的pH为5
D. 铵盐受热易分解
②下列方法中,可以使氨水电离程度增大的是(填字母序号).
A.加入少量氯化铁固体 B.通入氨气
C.加入少量氯化铵固体 D.加水稀释
(2)盐酸和醋酸是中学常见酸 用0.1molL﹣1NaOH溶液分别滴定体积均为20.00mL、浓度均为0.1molL﹣1的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线.
①滴定醋酸的曲线是(填“I”或“II”).
②滴定开始前,三种溶液中由水电离出的c(H+)最大的是 .
③V1和V2的关系:V1V2(填“>”、“=”或“<”).
④M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是 .
(3)常温下将0.2mol/L HCl溶液与0.2mol/L氨水溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,求混合溶液中下列算式的精确计算结果(填具体数字): c(H+)﹣c(NH3﹒H2O)=mol/L.
(4)铵盐和氯化银是中学常见盐 ①0.1molL﹣1的(NH4)2Fe(SO4)2溶液,与同浓度的(NH4)2SO4溶液相比较(填溶质的化学式)溶液中NH4+的浓度更大,其原因是
②含有足量AgCl固体的饱和溶液,AgCl在溶液中存在如下平衡:
AgCl(s)Ag+(aq)+Cl﹣(aq)
在25℃时,AgCl的Ksp=1.8×10﹣10 . 现将足量AgCl分别放入下列液体中:
①100mL蒸馏水
②100mL 0.3molL﹣1AgNO3溶液
③100mL 0.1molL﹣1 MgCl2溶液
充分搅拌后冷却到相同温度,Ag+浓度由大到小的顺序为(填序号).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】针对网络上流传的隔夜熟肉中因亚硝酸钠(NaNO2)含量严重超标而不能食用的说法,某兴趣小组开展如下探究活动: 活动一:查阅资料:NaNO2有毒,溶液显碱性,NaNO2有较强的氧化性和较弱的还原性.国家规定肉制品中NaNO2含量不能超过30mg/kg.
(1)NaNO2溶液显碱性的原因是 . (用离子方程式表达) 活动二:鉴别NaNO2与食盐
(2)可用稀硫酸、淀粉和KI溶液鉴别,溶液变蓝的是 . (填化学式).
(3)活动三:检测熟肉中NaNO2含量的变化 分别从 1000g刚煮熟的肉和 1000g隔夜熟肉中提取NaNO2 , 配成溶液,再分别用0.00500mol/L酸性高锰酸钾溶液滴定,刚煮熟的肉消耗12.00mL,隔夜熟肉消耗16.00mL.(提示:MnO4-转化为Mn2+ , NO2-转化为NO3-)
①在做该滴定实验时需要用到的实验仪器有
A.容量瓶 B.酸式滴定管 C.碱式滴定管D.分液漏斗 E.锥形瓶 F. 烧瓶
②滴定终点的判断依据为 .
③隔夜熟肉中NaNO2的含量是mg/kg (保留三位有效数字),该数据说明保存得当的隔夜熟肉(选填“能”或“不能”)食用.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸乙烯(CH3COOCH=CH2)是一种重要的有机化工原料,以二甲醚(CH3OCH3)与合成气(CO、H2)为原料,醋酸锂、碘甲烷等为催化剂,在高压反应釜中一步合成醋酸乙烯及醋酸。
回答下列问题:
(1)常温下,将浓度均为a mol/L的醋酸锂溶液和醋酸溶液等体积混合,测得混合液的pH=b,则混合液中c(CH3COO-)=______mol/L( 列出计算式即可)。
(2)合成二甲醚:
Ⅰ.2H2(g)+CO(g)=CH3OH(g) ΔH1=-91.8kJ/mol;
Ⅱ.2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH2=-23.5 kJ/mol;
Ⅲ.CO(g)+H2O(g)=CO2(g)+H2(g) ΔH3=-41.3 kJ/mol.
已知:H-H 的键能为436kJ/mol,C=O的键能为803kJ/mol,H-O的键能为464kJ/mol,则C≡O的键能为_____kJ/mol.
(3)二甲醚(DME)与合成气一步法合成醋酸乙烯(VAC)的反应方程式为2CH3OCH3(g)+4CO(g)+H2(g) ![]() CH3COOCH=CH2(g)+2CH3COOH(g),T℃时,向2L恒容密闭反应釜中加入0.2 molCH3OCH3、0.4 molCO、0.1molH2发生上述反应,10min达到化学平衡,测得VAC的物质的量分数为10%。
CH3COOCH=CH2(g)+2CH3COOH(g),T℃时,向2L恒容密闭反应釜中加入0.2 molCH3OCH3、0.4 molCO、0.1molH2发生上述反应,10min达到化学平衡,测得VAC的物质的量分数为10%。
①0~10min内,用CO浓度变化表示的平均反应速率v(CO)=______;该温度下,该反应的平衡常数K=__________。
②下列能说明该反应达到平衡状态的是______(填选项字母)。
A.V正(DME)=v逆(H2)≠0
B.混合气体的密度不再变化
C.混合气体的平均相对分子质量不再变化
D.c(CO):c(VAC)=4:1
③如图是反应温度对二甲醚(DME)的转化率和醋酸乙烯(VAC)选择性(醋酸乙烯的选择性Svac=![]() )的影响,该反应的ΔH______0(填“>”“<”或“=”);控制的最佳温度是___________.
)的影响,该反应的ΔH______0(填“>”“<”或“=”);控制的最佳温度是___________.

④保持温度不变,向反应釜中通入氩气增大压强,则化学平衡______(填“向正反应方向”“向逆反应方向"或“不”)移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2008年北京奥运会的“祥云”火炬所用燃料的主要成分是丙烷,下列有关丙烷的叙述正确的是( )
A. 是天然气的主要成分 B. 光照下能够发生取代反应
C. 与丁烷互为同分异构体 D. 分子中碳原子在一条直线上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示的装置进行电解.通电一会儿,发现用NaCl溶液湿润的淀粉KI试纸的C端变为蓝色. 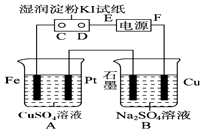
(1)E为电源的极,Fe为极.
(2)A中发生反应的离子方程式为 , B中发生反应的化学方程式为 .
(3)在B中观察到的现象是
(4)若此电源为铅蓄电池,电池总反应式为: Pb+PbO2+4H++2SO42﹣ ![]() PbSO4+2H2O
PbSO4+2H2O
则放电时:正极的电极反应式是;充电时:阴极的电极反应式是;当外电路通过1mol电子时,理论上负极板的质量增加g,此时若要使A池中的溶液复原,应加入g的CuO固体.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com