
·ÖĪö ŅŅČ²²»ÓėNaOHČÜŅŗ·“Ó¦£¬µ«Įņ»ÆĒāÄÜÓė¼ī·“Ó¦£¬¹ŹŅŅČ²µÄ¼ģŃéÓ¦·ÅŌŚÅųżĮņ»ÆĒāµÄøÉČÅŗó½ųŠŠ£¬Ń”ĶعżĮņĖįĶČÜŅŗÉś³ÉŗŚÉ«³Įµķ¼ģŃéĮņ»ÆĒāµÄ“ęŌŚ£»ŌŁĶعżNaOHČÜŅŗ³żČ„Įņ»ÆĒā£¬ŌŁĶعżĮņĖįĶČÜŅŗČ·ČĻĮņ»ÆĒāŅŃ³żøɾ»£®×īŗóÓĆøßĆĢĖį¼ŲĖįŠŌČÜŅŗĶŹÉ«ŹµŃé¼ģŃéŅŅČ²£¬
£Ø1£©ŹµŃéŹŅÖĘČ”ŅŅČ²³£Ņņŗ¬ŌÓÖŹÉś³ÉÉŁĮæH2S£¬ŹµŃéŅŌČ·Ö¤ÉĻŹö»ģŗĻĘųĢåÖŠŗ¬ÓŠŅŅČ²ŗĶH2S£¬ĻČ¼ģŃéĮņ»ÆĒāµÄ“ęŌŚÓĆĮņĖįĶČÜŅŗ¼ģŃ飬ĶعżĒāŃõ»ÆÄĘČÜŅŗ³żČ„Įņ»ÆĒā£¬ĶعżĮņĖįĶČÜŅŗ¼ģŃéĮņ»ÆĒāŹĒ·ń³ż¾»£¬×īŗóÓĆøßĆĢĖį¼ŲČÜŅŗ»ņäåĖ®¼ģŃéŅŅČ²µÄ“ęŌŚ£¬
£Ø2£©Įņ»ÆĒāŹĒ·ń“ęŌŚæÉÓĆĮņĖįĶČÜŅŗ¼ģŃ飻
£Ø3£©×°ÖĆBŹĒ³żČ„Įņ»ÆĒā£»
£Ø4£©ĄūÓĆĮņĖįĶČÜŅŗ¼ģŃéĮņ»ÆĒāŹĒ·ń³ż¾»£»
£Ø5£©¼ģŃéŅŅČ²æÉŅŌÓĆäåĖ®»ņøßĆĢĖį¼ŲĖįŠŌČÜŅŗ£»ŅŅČ²ŗĶ¶žŃõ»ÆĮņ¶¼ÄÜŹ¹äåĖ®»ņøßĆĢĖį¼ŲĖįŠŌČÜŅŗĶŹÉ«£®
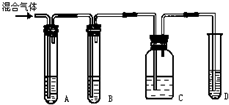
½ā“š ½ā£ŗ£Ø1£©ŹµŃéŹŅÖĘČ”ŅŅČ²³£Ņņŗ¬ŌÓÖŹÉś³ÉÉŁĮæH2S£¬ŹµŃéŅŌČ·Ö¤ÉĻŹö»ģŗĻĘųĢåÖŠŗ¬ÓŠŅŅČ²ŗĶH2S£¬ĻČ¼ģŃéĮņ»ÆĒāµÄ“ęŌŚÓĆĮņĖįĶČÜŅŗ¼ģŃ飬ĶعżĒāŃõ»ÆÄĘČÜŅŗ³żČ„Įņ»ÆĒā£¬ĶعżĮņĖįĶČÜŅŗ¼ģŃéĮņ»ÆĒāŹĒ·ń³ż¾»£¬×īŗóÓĆøßĆĢĖį¼ŲČÜŅŗ»ņäåĖ®¼ģŃéŅŅČ²µÄ“ęŌŚ£¬ČēĶ¼ĖłŹ¾A”¢B”¢C”¢D×°ÖĆÖŠæÉŹ¢·ÅµÄŹŌ¼ĮŹĒ¢Ł”¢¢Ś”¢¢Ł”¢¢Ü»ņ¢Ū£¬
¹Ź“š°øĪŖ£ŗ¢Ł£»¢Ś£»¢Ł£»¢Ü»ņ¢Ū£»
£Ø2£©Įņ»ÆĒāŹĒ·ń“ęŌŚæÉÓĆĮņĖįĶČÜŅŗ¼ģŃ飬ÄÜĖµĆ÷H2SĘųĢå“ęŌŚµÄĻÖĻóŹĒÉś³ÉŗŚÉ«³Įµķ£¬CuSO4+H2S=CuS”ż+H2SO4£¬
¹Ź“š°øĪŖ£ŗ×°ÖĆAÖŠÓŠŗŚÉ«³Įµķ£»
£Ø3£©×°ÖĆBŹĒ³żČ„³żČ„H2SĘųĢ壬ŅŌĆāøÉČÅŅŅČ²µÄŠŌÖŹŹµŃ飬
¹Ź“š°øĪŖ£ŗ³żČ„H2SĘųĢ壬ŅŌĆāøÉČÅŅŅČ²µÄŠŌÖŹŹµŃ飻
£Ø4£©ĄūÓĆ×°ÖĆCÖŠĮņĖįĶČÜŅŗµÄÄæµÄŹĒ¼ģŃéĮņ»ÆĒāŹĒ·ń³ż¾»£¬ČōĪŽŗŚÉ«³ĮµķÖ¤Ć÷Įņ»ÆĒā³ż¾»£¬
¹Ź“š°øĪŖ£ŗ¼ģŃéH2SŹĒ·ń³ż¾”£»
£Ø5£©¼ģŃéŅŅČ²æÉŅŌÓĆäåĖ®»ņøßĆĢĖį¼ŲĖįŠŌČÜŅŗ£¬ŅŅČ²ŗĶ¶žŃõ»ÆĮņ¶¼ÄÜŹ¹äåĖ®»ņøßĆĢĖį¼ŲĖįŠŌČÜŅŗĶŹÉ«£¬Č·Ö¤ŗ¬ÓŠŅŅČ²µÄĻÖĻóŹĒ×°ÖĆC֊ƻӊŗŚÉ«³Įµķ£¬×°ÖĆDÖŠµÄČÜŅŗĶŹÉ«£¬
¹Ź“š°øĪŖ£ŗ×°ÖĆC֊ƻӊŗŚÉ«³Įµķ£¬×°ÖĆDÖŠµÄČÜŅŗĶŹÉ«£®
µćĘĄ ±¾Ģāæ¼²éŅŅČ²µÄ»ÆѧŠŌÖŹ”¢ÖʱøŅŌ¼°³£¼ūĘųĢåµÄ¼ģŃ飬ĢāÄæÄѶČÖŠµČ£¬×¢ŅāŹµŃéµÄĻČŗóĖ³Šņ£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ¼ÓČėÉŁĮæĻ”ĮņĖį | B£® | ¼ÓČČ | ||
| C£® | ¼ÓÕōĮóĖ® | D£® | ¼ÓČėÉŁĮæĮņĖįĶČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®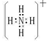 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·²ŹĒŗ¬ÓŠĢ¼ŌŖĖŲµÄ»ÆŗĻĪļ¶¼ŹōÓŚÓŠ»śĪļ | |
| B£® | “󶹏żÓŠ»śĪļ¶¼ŹĒÓÉ·Ö×Ó¹¹³ÉµÄ | |
| C£® | ÓŠ»śĪļ¶¼ŗÜČŻŅ×Č¼ÉÕ | |
| D£® | Ņ×ČÜÓŚĘūÓĶ”¢¾Ę¾«”¢±½µČÓŠ»śČܼĮÖŠµÄĪļÖŹ£¬Ņ»¶ØŹĒÓŠ»śĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
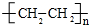 £¬ŹĒĖÜĮĻµÄÖ÷ŅŖ³É·Ö£ŗ
£¬ŹĒĖÜĮĻµÄÖ÷ŅŖ³É·Ö£ŗ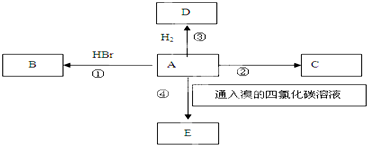
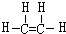 £¬DµÄ·Ö×ÓŹ½ĪŖC2H6£»DÄÜŌŚ¹āÕÕĢõ¼žĻĀÓėĀČĘų·¢ÉśČ”“ś·“Ó¦
£¬DµÄ·Ö×ÓŹ½ĪŖC2H6£»DÄÜŌŚ¹āÕÕĢõ¼žĻĀÓėĀČĘų·¢ÉśČ”“ś·“Ó¦²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  ¹ā·ü·¢µē | B£® |  ·ēĮ¦·¢µē | C£® |  ¹āŗĻ×÷ÓĆ | D£® | 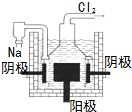 µē½āÖĘÄĘ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ū¢Ü¢Ž¢ß | B£® | ¢Ś¢Ū¢Ż¢ß | C£® | ¢Ś¢Ż¢ß | D£® | ¢Ś¢Ü¢Ż¢ß |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
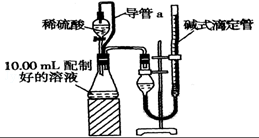 ŹµŃéŹŅ²ā¶ØĢ¼ĖįÄĘŗĶĢ¼ĖįĒāÄĘ»ģŗĻĪļÖŠĢ¼ĖįÄʵÄÖŹĮæ·ÖŹżW£ØNa2CO3£©£¬³ĘČ”“Ė»ģŗĻĪļ5.0g£¬ČÜÓŚĖ®ÖŠ£¬Åä³É250mLČÜŅŗ
ŹµŃéŹŅ²ā¶ØĢ¼ĖįÄĘŗĶĢ¼ĖįĒāÄĘ»ģŗĻĪļÖŠĢ¼ĖįÄʵÄÖŹĮæ·ÖŹżW£ØNa2CO3£©£¬³ĘČ”“Ė»ģŗĻĪļ5.0g£¬ČÜÓŚĖ®ÖŠ£¬Åä³É250mLČÜŅŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | OH- | B£® | H3O+ | C£® | CH4 | D£® | HF |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com