
 .
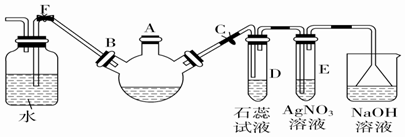
.分析 实验室制备溴苯是用苯和液溴在铁粉作催化剂的条件下发生取代反应生成溴苯和溴化氢,根据装置图可知,生成溴苯的同时还有溴化氢生成另外还有少部分溴挥发,所以在D装置中盛放石蕊检验HBr,E中的硝酸银会产生溴化银沉淀,尾气用氢氧化钠溶液吸收,关闭C打开F时,由于溴化氢极易溶于水,广口瓶中的水会倒吸入三颈烧瓶,
(1)根据溴苯的性质可知,溴苯是一种密度比水大的无色液体,在实验中因为溶解了大量的溴而显褐色,在三口烧瓶中铁与溴生成溴化铁,苯与溴在溴化铁作催化剂的条件下了生取代反应生成溴苯和溴化氢;
(2)根据溴化氢易挥发显酸性分析;溴化氢气体通入硝酸银溶液,能产生浅黄色沉淀;
(3)溴化氢极易溶于水,容易发生倒吸,溴苯不溶于水;
(4)三口烧瓶中的溴苯含有少量的溴和溴化氢,可以用NaOH溶液除去.
解答 解:(1)在三口烧瓶中铁与溴生成溴化铁,苯与溴在溴化铁作催化剂的条件下了生取代反应生成溴苯和溴化氢,所以发生反应的化学方程式为: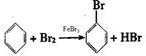 ,
,
故答案为: ;
;
(2)苯与溴在溴化铁作催化剂的条件下了生取代反应生成溴苯和溴化氢,溴化氢易挥发显酸性,则试管D中看到的现象为有白雾产生,试液变红;溴化氢溶于水和硝酸银反应生成溴化银淡黄色的,则试管E中现象为:出现淡黄色沉淀,故答案为:有白雾产生,试液变红;出现淡黄色沉淀;
(3)由于溴化氢极易溶于水,所以待三颈烧瓶中的反应进行到仍有气泡冒出时打开F夹,关闭C夹,可以看到的现象是与B相连的广口瓶中水倒吸入三颈烧瓶,溴苯不溶于水,所以三口烧瓶中会出现分层,
故答案为:广口瓶中的水沿导管倒吸入三颈烧瓶中,烧瓶中液体出现分层;
(4)三口烧瓶中的溴苯中含有少量的溴,可以用NaOH溶液除去,反应离子方程式为:Br2+2OH-═Br-+BrO-+H2O;
故答案为:Br2+2OH-═Br-+BrO-+H2O.
点评 本题通过溴苯的制备,考查了制备方案的设计方法,为高考常见题型,题目难度中等,试题综合性强,难易适中,在注重对学生基础性知识考查和训练的同时,侧重对学生能力的培养和解题方法的指导与训练,有利于培养学生的严谨规范的实验设计能力,也有利于提高学生的学科素养.


 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源: 题型:选择题
| A. | 已知甲烷的燃烧热为890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)=2CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| C. | 已知中和热为△H=-57.4 kJ•mol-1,则1mol稀硫酸和足量稀NaOH溶液反应的反应热就是中和热 | |
| D. | CO(g)的燃烧热是283.0 kJ•mol-1,则2CO2(g)═2CO(g)+O2(g)反应的△H=+(2×283.0)kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | a |
| A | B | C | D | |
| c(CO2) | 3 | 1 | 0.8 | 1 |
| c(H2) | 2 | 1 | 0.8 | 1 |
| c(CO) | 1 | 2 | 3 | 0.5 |
| c(H2O) | 2 | 2 | 3 | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加催化剂,v正、v逆都发生变化,且变化的倍数相等 | |
| B. | 加压,v正、v逆都增大,且v正增大的倍数大于v逆增大的倍数 | |
| C. | 降温,v正、v逆都减小,且v正减小的倍数大于v逆减小的倍数 | |
| D. | 增大氮气的浓度,v正增大、v逆不变,N2转化率减小,H2转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | 实验操作 | |
| A | 制备Fe(OH)3胶体 | 将NaOH浓溶液滴加到饱和FeCl3溶液中 |
| B | 由MgCl2溶液制备无水MgCl2 | 将MgCl2溶液加热蒸干 |
| C | 除去Cu粉中混有的CuO | 加入稀硝酸,过滤、洗涤、干燥 |
| D | 用CCl4萃取碘水中的I2 | 先从分液漏斗下口放出有机层,然后从上口倒出水层 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO32-、Cl-、OH- | B. | Cl-、OH-、CO32- | C. | OH-、Cl-、CO32- | D. | CO32-、OH-、Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com