
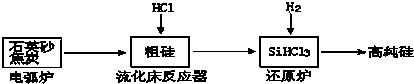
分析 (1)在提纯粗硅的流程中硅元素被还原一步为四氯化硅与氢气反应生成硅与氯化氢;
(2)铜与三价铁离子发生氧化还原反应生成二价铁离子和铜离子;
(3)铝性质活泼,能够与空气中氧气发生反应生成氧化铝,生成一层致密氧化膜,阻止铝与空气接触,铝镁形成合金也能与氧气反应生成氧化膜阻止反应进行.
解答 解:I.(1)在提纯粗硅的流程中硅元素被还原一步为四氯化硅与氢气反应生成硅与氯化氢,化学方程式:SiCl4+2H2=Si+4HCl;
故答案为:SiCl4+2H2=Si+4HCl;
(2)铜与三价铁离子发生氧化还原反应生成二价铁离子和铜离子,离子方程式:Cu+2Fe3+=2Fe2++Cu2+;
故答案为:Cu+2Fe3+=2Fe2++Cu2+;
(3)铝性质活泼,能够与空气中氧气发生反应生成氧化铝,生成一层致密氧化膜,阻止铝与空气接触,铝镁形成合金也能与氧气反应生成氧化膜阻止反应进行,所以合金中的铝在空气中不易被腐蚀;
a.铝性质活泼,能够与空气中氧气发生反应,故a不选;
b.铝金属的表面存在一层致密的氧化膜氧化铝,氧化铝能阻止氧气与铝接触,防止腐蚀,故b选;
c.铝镁形成合金也能与氧气反应生成氧化镁、氧化铝氧化膜阻止反应进行,能够防止腐蚀,故c选;
故选:bc.
点评 本题考查了方程式、离子方程式的书写,铝及合金的性质,明确反应实质及铝的性质是解题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
| 物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| 沸点/℃ | 2 355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
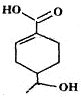
| A. | 分子中含有四种官能团 | |
| B. | 1mol该有机物完全燃烧消耗O2的物质的量为10mol | |
| C. | 能发生加成、取代、消去、水解等反应 | |
| D. | 相同条件下,等量的该有机物分别与足量的Na和NaHCO3溶液反应产生的气体的量相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.
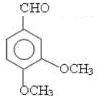 ;
; ;
;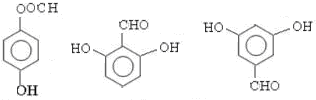 任意一种;(任写一种)
任意一种;(任写一种)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 宇宙星体、地球内部都处于高压状态,探究“高压下钠和锂单质金属→绝缘体转变”现象的本质、理解处于高压状态下一些物质的行为具有重要意义,它们可以为研究星体和地球内部构造提供理论支持 | |
| B. | 工业、农业以及日常生活中产生的污水应当分开处理.常用的污水处理方法有中和法、氧化还原法、离子交换法、萃取法、吹脱法、吸附法、电渗析法等,其中前三种属于化学处理方法 | |
| C. | 新型炸药--C4塑胶炸药得名于其空间网状延展结构的每个结构基元含有4个碳原子,由于该炸药成体时无需包裹金属外壳及添加金属芯件,因此能轻易躲过普通X光安全检查,具有较强的隐蔽性 | |
| D. | 建筑领域常使用的黏土、石英、白垩石和多用于农业和食品工业的硅藻土、硅胶均不属于硅酸盐材料的范畴 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙二醇和丙三醇互为同系物 | |
| B. | 不同元素的原子构成的分子只含极性共价键 | |
| C. | ${\;}_{92}^{235}$U和${\;}_{92}^{238}$U是中子数不同质子数相同的同种核素 | |
| D. | 短周期第ⅣA与ⅦA族元素的原子间构成的分子,均满足原子最外层8电子结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | b、c与a形成化合物的稳定性一定为c>b | |
| B. | a和d形成的化合物与水反应产生气体可以作燃料 | |
| C. | c、a和b可形成的化合物为离子化合物 | |
| D. | a、b、c、d四种元素组成的化合物的水溶液可以为酸性、也可以为碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫化橡胶 | B. | 酚醛树脂 | C. | 聚乙烯塑料 | D. | 硝酸纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
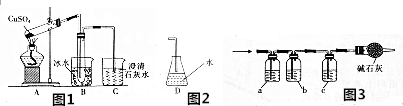
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com