
| A. | 乙炔 | B. | 丙炔 | C. | 丁炔 | D. | 1,3-丁二烯 |
分析 由选项可知,都是链烃,0.5体积某气态烃和与1体积氯气发生加成反应,说明分子中含2个双键或1个C≡C.生成了0.5体积该卤代烷能和3体积氯气发生取代反应,说明1个卤代烷中含有6个H原子,加成时1个烃分子已引入2个H原子形成卤代烷,所以该气体烃分子中含有4个H原子,以此来解答.
解答 解:由选项可知,都是链烃,0.5体积某气态烃和与1体积氯气发生加成反应,说明分子中含2个双键或1个C≡C.生成了0.5体积该卤代烷能和3体积氯气发生取代反应,说明1个卤代烷中含有6个H原子,加成时1个烃分子已引入2个H原子形成卤代烷,所以该气体烃分子中含有4个H原子,
由选项可知,都是链烃,故该气态烃分子中C原子数目为$\frac{4+2}{2}$=3,故ACD错误,B正确,
故选B.
点评 本题考查有机物分子式的确定,难度不大,理解加成反应与取代反应是解题关键.


 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:解答题
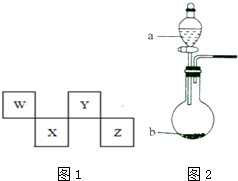 W、X、Y、Z四种短周期元素在周期表中的位置如图1所示,其中Y与钠元素和氢元素均可形成原子个数1:1和1:2的化合物.
W、X、Y、Z四种短周期元素在周期表中的位置如图1所示,其中Y与钠元素和氢元素均可形成原子个数1:1和1:2的化合物.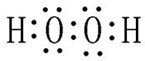 ,Z在周期表中的位置第三周期ⅦA族.
,Z在周期表中的位置第三周期ⅦA族.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO2、CH4、NaOH、MgO | B. | Cl2、NH3•H20、NaOH、Si02 | ||
| C. | Ca、Ma2C03、H2Si03、MgO | D. | NO2、CH4、H2SiO3、SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;取代反应
;取代反应 ;加成反应
;加成反应 ;取代反应
;取代反应查看答案和解析>>
科目:高中化学 来源: 题型:选择题
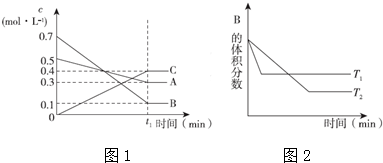
| A. | 该平衡体系的化学反应方程式为:3A(g)+B(g)═4 C(g) | |
| B. | 在t1时间内用B表示该反应的平均速率为0.6/t1mol•L-1•min-1 | |
| C. | 其他条件不变,升高温度,正反应速率减小、逆反应速率增大,A的转化率减小 | |
| D. | 维持温度和容器体积不变,往平衡体系中充惰性气体,C的百分含量增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若Q1+Q2<Q3,则反应为放热反应 | B. | 若Q1+Q2>Q3,则反应为放热反应 | ||
| C. | 若E1+E2>E3,则反应为吸热反应 | D. | 若E1+E2>E3,则Q1+Q2>Q3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两种溶液pH的大小顺序是②>① | |
| B. | 若将两种溶液稀释相同倍数,pH变化较大的是② | |
| C. | 若分别加入25mL0.1mol•L-1盐酸后,pH较大的是① | |
| D. | 若两种溶液的pH均为9,则物质的量浓度大小关系是①>② |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com