
| A、60% | B、>60% |
| C、<60% | D、无法确定 |
| m(溶质) |
| m(溶液) |
| V(30%ρ1+90%ρ2)g |
| V(ρ1+ρ2)g |
| 30%ρ1+90%ρ2 |
| ρ1+ρ2 |


科目:高中化学 来源: 题型:
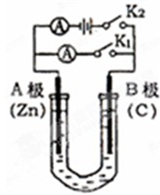 如图所示,U形管内盛有100mL的溶液,请按要求回答下列回答.
如图所示,U形管内盛有100mL的溶液,请按要求回答下列回答.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、⑤④①③⑦⑥② |
| B、②⑥⑦③①⑤④ |
| C、④⑤①③⑦⑥② |
| D、②⑥⑦③①④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用甲醛溶液浸泡水产品以延长保质期 |
| B、在饲料中添加“瘦肉精”以增加猪肉的瘦肉含量 |
| C、高层住房着火.立即打开所有门窗 |
| D、燃着的酒精灯不慎碰到,立即用湿布盖灭 |
查看答案和解析>>
科目:高中化学 来源: 题型:
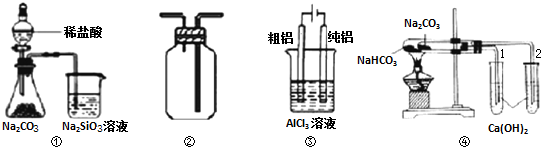
| A、用图①装置验证氯、碳、硅元素非金属性 |
| B、用图②装置能收集O2、CO2和H2 |
| C、用图③装置电解精炼铝 |
| D、用图④装置验证NaHCO3和Na2CO3的热稳定性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④ | B、①③④② |
| C、①④②③ | D、①④③② |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1L该溶液中含KNO3101g | ||
B、100mL该溶液中含N
| ||
| C、从1L该溶液中取出100mL,所取出的KNO3溶液的浓度为0.01mol/L | ||
| D、在1L水中溶解10.1g KNO3,即可配制得0.1mol/L KNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、③⑤ | B、①②④ |
| C、全部正确 | D、②④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com