
【题目】将足量的AgCl(s)分别添加到下述四种溶液中,所得溶液c(Ag+)最小的是
A.10 mL 0.4mol·L-1的盐酸B.10 mL 0.3mol·L-1MgCl2溶液
C.10 mL 0.5mol·L-1NaCl溶液D.10 mL 0.1mol·L-1AlCl3溶液
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.在氢原子的电子云图中,每个小黑点代表一个电子
B.某基态原子3d能级中电子排布的情况可能为 ![]()
C.电子构型为[Ar]3d104s2的元素是过渡金属元素
D.当碳原子的核外电子排布由1s22s22p2转变为1s22s12p3时,碳原子由基态变为激发态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M是聚合物胶黏剂、涂料等的单体,其一条合成路线如下(部分试剂及反应条件省略):
完成下列填空:
(1)反应①的反应类型是 . 反应④的反应条件是 .
(2)除催化氧化法外,由A得到 ![]() 所需试剂为 .
所需试剂为 .
(3)已知B能发生银镜反应.由反应②、反应③说明:在该条件下, .
(4)写出结构简式,C;M
(5)D与1﹣丁醇反应的产物与氯乙烯共聚可提高聚合物性能,写出该共聚物的结构简式.
(6)写出一种满足下列条件的丁醛的同分异构体的结构简式.等
①不含羰基②含有3种不同化学环境的氢原子
已知:双键碳上连有羟基的结构不稳定.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知硫酸、氨水的密度与所加水的量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
溶质的物质的量浓度/molL﹣1 | 溶液的密度/gcm﹣3 | |
硫酸 | c1 | ρ1 |
氨水 | c2 | ρ2 |

(1)表中硫酸的质量分数为(不写单位,用含c1、ρ1 , 的代数式表示).
(2)物质的量浓度为c1molL﹣1的硫酸与水等体积混合(混合后溶液的体积变化忽略不计),所得溶液的物质的量浓度为molL﹣1 .
(3)将物质的量浓度分别为c2molL﹣1和 ![]() c2molL﹣1的氨水等质量混合,所得溶液的密度(填“大于”、“小于”或“等于”,下同)ρ2gcm﹣3 , 所得溶液的物质的量浓度
c2molL﹣1的氨水等质量混合,所得溶液的密度(填“大于”、“小于”或“等于”,下同)ρ2gcm﹣3 , 所得溶液的物质的量浓度 ![]() c2molL﹣1(设混合后溶液的体积变化忽略不计)
c2molL﹣1(设混合后溶液的体积变化忽略不计)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水热法制备纳米颗粒Y的反应是3Fe2++2S2O32﹣+O2+XOH﹣═Y+S4O62﹣+2H2O,下列说法中,正确的是( )
A.Y的化学式为Fe2O3
B.x=6
C.1mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为 ![]() mol
mol
D.每生成1mol Y,反应转移的电子总数为4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】油脂能增加食物的滋味,增进食欲,保证机体的正常生理功能.但摄入过量脂肪,可能引起肥胖、高血脂、高血压等.下列食品中富含油脂的是( )
A.苹果
B.大米
C.白菜
D.花生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化钠是日常生活的必需品,也是重要的化工原料.粗盐除含NaCl外,还含有少量MgCl2、CaCl2、Na2SO4以及泥沙等杂质.以下是粗盐提纯的操作流程.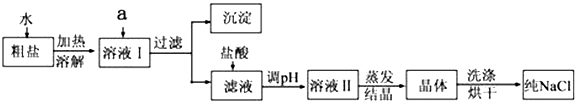
提供的试剂:Na2CO3溶液、K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、饱和NaCl溶液、稀盐酸.
(1)欲除去溶液I中的MgCl2、CaCl2、Na2SO4 , 从提供的试剂中选出a所代表的试剂,试剂的选择和滴加顺序均正确的是:;
A.Na2CO3溶液、BaCl2溶液、NaOH溶液
B.溶液、NaOH溶液、K2CO3溶液
C.NaOH溶液、BaCl2溶液、Na2CO3溶液
D.Ba(NO3)2、NaOH溶液、Na2CO3溶液
E.BaCl2溶液、Na2CO3溶液、NaOH溶液
(2)过量碳酸盐溶液的作用是 .
(3)洗涤晶体操作使用的玻璃仪器有 .
(4)蒸发结晶的操作方法是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2C2O4为二元弱酸.20℃时,配制一组c(H2C2O4)+c(HC2O4﹣)+c(C2O42﹣)=0.100molL﹣1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示.下列指定溶液中微粒的物质的量浓度关系一定正确的是( ) 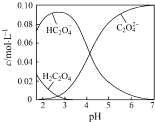
A.pH=2.5的溶液中:c(H2C2O4)+c(C2O42﹣)>c(HC2O4﹣)
B.c(Na+)=0.100 molL﹣1的溶液中:c(H+)+c(H2C2O4)=c(OH﹣)+c(C2O42﹣)
C.c(HC2O4﹣)=c(C2O42﹣)的溶液中:c(Na+)>0.100 molL﹣1+c(HC2O4﹣)
D.pH=7的溶液中:c(Na+)>2c(C2O42﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型净水剂高铁酸钾(K2FeO4)为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液中稳定.生产K2FeO4的工艺流程如图所示: 
(1)写出“氧化”过程中生成Na2FeO4的化学方程式: .
(2)“转化”过程中发生反应的化学方程式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com