
【题目】化学平衡状态Ⅰ、Ⅱ、III的相关数据如下表:
编号 | 化学方程式 | 平衡常数 | 温度 | |
979K | 1173K | |||
Ⅰ | Fe(s)+CO2(g) FeO(s)+ CO(g) | K1 | 1.47 | 2.15 |
Ⅱ | CO(g)+H2O(g) CO2(g)+H2(g) | K2 | 1.62 | b |
Ⅲ | Fe(s)+ H2O(g) FeO(s) +H2(g) | K3 | a | 1.68 |
根据以上信息判断,下列结论正确的是
A.a<b
B.反应Ⅱ、III均为放热反应
C.升高温度平衡状态III向正反应方向移动
D.增大压强,状态Ⅱ正反应速率增大,逆反应速率减小,平衡不移动
【答案】B
【解析】
Fe(s)+CO2FeO(s)+CO(g),K1=![]() ,
,
CO(g)+H2O(g)CO2(g)+H2(g),K2=![]() ,
,
Fe(s)+H2O(g)FeO(s)+H2(g),K3=![]() ,
,
同温度下,K2=![]() ,K3=K1K2,979K平衡常数a=1.47×1.62=2.38,1173K平衡常数b=
,K3=K1K2,979K平衡常数a=1.47×1.62=2.38,1173K平衡常数b=![]() =0.78;
=0.78;
A.计算分析可知a>b,故A错误;
B.反应Ⅱ的平衡常数随温度升高减小,说明正反应为放热反应,反应Ⅲ平衡常数随温度升高减小,说明正反应为放热反应,故B正确;
C.有计算得到两种不同温度下的平衡常数可知,反应Ⅲ平衡常数随温度升高减小,平衡逆向进行,故C错误;
D.反应ⅡCO(g)+H2O(g)CO2(g)+H2(g),是气体体积不变的反应,增大压强正逆反应速率均增大,但平衡不动,故D错误;
故答案为B。


 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:
【题目】温度为T时,向2.0L恒容密闭容器中充入1.0molA,反应A(g)===B(g)+C(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表:下列说法正确的是
t/s | 0 | 50 | 150 | 250 | 350 |
n(B)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A. 反应在前50s的平均速率v(B)=0.0032mol·L-1·s-1
B. 保持其他条件不变,升高温度,平衡时c(B)=0.11mol·L-1,则反应的ΔH<0
C. 相同温度下,起始时向容器中充入1.0mol A、0.20mol B和0.20mol C,反应达到平衡前v正<v逆
D. 相同温度下,起始时向容器中充入2.0mol B和2.0mol C,达到平衡时,B的转化率大于80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型钠硫电池结构示意图如图,下列有关该电池的说法正确的是

A.电池放电时,Na+向电极A极移动
B.电池放电时,A极电极反应为2Na++xS+2e-= Na2Sx
C.电池充电时,B接负极
D.电池充电时,每转移1mol电子将有1mol Na+被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮(N)、磷(P)、砷(As)等都是VA族的元素,该族元素的化合物在研究和生产中有许多重要用途。回答下列问题:
(1)NH3的沸点比PH3高,原因是________________________________________________。
(2)Na3AsO4 中含有的化学键类型包括________________________;AsO43-的空间构型为____________(用文字描述)。
(3)NH3和F2在Cu催化下可发生反应4NH3+3F2=NF3+3NH4F,化学方程式中的5种物质所属的晶体类型有_____________________(填序号)。写出基态铜原子的价电子排布式_______________。
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同周期的X、Y、Z三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序是:HZO4![]() H2YO4
H2YO4 ![]() H3XO4,下列判断正确的是 ( )
H3XO4,下列判断正确的是 ( )
①阴离子的还原性按X、Y、Z顺序减弱
②单质的氧化性按X、Y、Z顺序增强
③元素的原子半径按X、Y、Z顺序减小
④气态氢化物的稳定性按X、Y、Z顺序减弱
①②A. ②③ B. ①②③ C. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个不导热的恒容密闭容器中通入CO(g)和H2O(g),一定条件下使反应CO(g)+H2O(g)![]() CO2(g)+H2(g)达到平衡状态,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是
CO2(g)+H2(g)达到平衡状态,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是
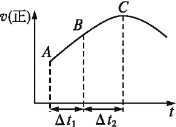
A.反应物浓度:A点小于C点
B.该反应的正反应为吸热反应
C.C点时反应进行的程度最大
D.Δt1=Δt2时,生成H2的物质的量:AB段小于BC段
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示为工业合成氨的流程图。有关说法错误的是

A. 步骤①中“净化”可以防止催化剂中毒
B. 步骤②中“加压”既可以提高原料的转化率,又可以加快反应速率
C. 步骤③、④、⑤均有利于提高原料的转化率
D. 产品液氨除可生产化肥外,还可用作制冷剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用以下几个实验装置探究电化学过程对金属与稀硫酸反应速率的影响,烧杯中都盛有稀H2SO4。试回答:
(1)B装置中Fe电极作为________(填“正”或“负”)极,电极反应式为______________;
(2)C装置中阳离子移向_________(填“Zn”或“Fe”)极;
(3)比较四个装置中Fe片被腐蚀的速率由快到慢的顺序是_______(用A、B、C、D表示)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com