
【题目】某化学课外兴趣小组为探究铜与浓硫酸的反应,用下图所示装置时行实验:
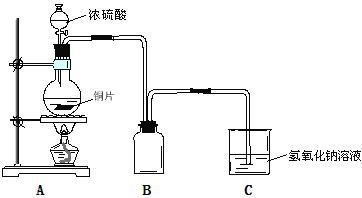

(1)B是用来收集实验中产生的气体的装置,装置图补充完整后正确的是__________;

(2)实验中他们取6.4g铜片和12mL 18mol·L-1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组中的同学认为还有一定量的硫酸剩余。
① 请写出铜跟浓硫酸反应的化学方程式:_____________________________________。
②下列试剂中,能证明反应停止后烧瓶中有硫酸剩余的是___________(填写字母编号)。
A.硫酸钠溶液 | B.BaCl2溶液 | C.银粉 | D.Na2CO3溶液 |
③为什么有一定量的硫酸剩余但未能使铜片完全溶解?你认为原因是__________________________。
(3)为了确定反应生成的主要气体成分,还可以在实验装置A和B之间补充以上右图D装置,其中洗气瓶中可以盛有__________(试剂)。
【答案】a Cu + 2H2SO4(浓)![]() CuSO4+ SO2↑+ 2H2O D 稀硫酸不与铜反应 品红溶液或酸性高锰酸钾或溴水
CuSO4+ SO2↑+ 2H2O D 稀硫酸不与铜反应 品红溶液或酸性高锰酸钾或溴水
【解析】
(1)SO2气体的密度比空气大,选择排空气法收集时,B装置中导气管长进短出,故答案为a;
(2)①铜与浓硫酸在加热条件下反应生成SO2的化学方程式为Cu + 2H2SO4(浓)![]() CuSO4+ SO2↑+ 2H2O;
CuSO4+ SO2↑+ 2H2O;
②因溶液里肯定有CuSO4存在,欲证明烧瓶内有硫酸存在,就要体现溶液里有H+存在,试剂应该能与酸反应,故选项D符合题意,现象是有气泡产生,选项A滴加后无现象,选项B滴加有白色沉淀,只能证明溶液里有SO42-,无法证明有硫酸,选项C银粉与硫酸溶液不反应,答案为D;
③随反应的进行,硫酸溶液的浓度逐渐降低,当成稀硫酸时,铜不与稀硫酸反应,因此溶液里会有铜剩余;
(3)因SO2有漂白性和还原性,因此可以在洗气瓶内盛放品红溶液或溴水或酸性高锰酸钾溶液。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】根据原子结构及元素周期律的知识,下列推断正确的是( )
A.同主族元素含氧酸的酸性随核电荷数的增加而减弱
B.核外电子排布相同的微粒化学性质也相同
C.Cl-、S2-、Ca2+、K+半径逐渐增大
D.![]() Cl与
Cl与![]() Cl得电子能力相同
Cl得电子能力相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甘氨酸亚铁[(NH2CH2COO)2Fe]是一种补铁强化剂。某学习小组利用FeCO3与甘氨酸(NH2CH2COOH)制备甘氨酸亚铁,实验装置如下图所示(夹持和加热仪器已省略)。
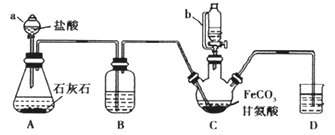
有关物质性质如下表
甘氨酸 | 柠檬酸 | 甘氨酸亚铁 |
易溶于水,微溶于乙醇 | 易溶于水和乙醇 | 易溶于水,难溶于乙醇 |
两性化合物 | 强酸性、强还原性 |
实验过程:
Ⅰ合成:装置C中盛有0.2 mol FeCO3和200 mL 1.0 mol·L1甘氨酸溶液和适量柠檬酸。实验时,先打开仪器a的活塞,待装置C中空气排净后,加热并不断搅拌,并通过仪器b向C中加入适量氢氧化钠溶液调节pH到6左右,使反应物充分反应。
Ⅱ分离:反应结束后,过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
回答下列问题:
(1)仪器C的名称是___________;与a相比,仪器b的优点是_______。
(2)装置B盛装的试剂为_____________。
(3)合成过程加入柠檬酸的作用是促进FeCO3溶解和______________。
(4)加入氢氧化钠溶液调节pH若大于6,甘氨酸亚铁产量下降。原因可用离子方程式表示为________________。
(5)过程II中洗涤操作为________。
(6)检验产品中是否含有Fe3+的最佳试剂是_________(写化学用语)。
(7)本实验制得15.3 g 甘氨酸亚铁(M=204g/mol),则其产率是_______%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列正确的叙述有
① CO2、SO2、P2O5均为酸性氧化物
②Ca(HCO3)2 、Fe(OH)3、FeCl2均可由化合反应制得
③ 碘晶体分散到酒精中、淀粉溶于水中所形成的分散系分别为:溶液、胶体
④ 灼热的炭与CO2的反应、Ba(OH)2·8H2O与NH4Cl的反应均属于氧化还原反应,又是吸热反应
⑤ 需要通电才可进行的有:电离、电解、电泳、电镀、电化学腐蚀
⑥ 氯化铁溶液与氢氧化铁胶体具有的共同性质是:能透过滤纸,加热蒸干、灼烧后都有氧化铁生成
⑦ 按照纯净物、混合物、强电解质、弱电解质和非电解质顺序排列的是CuSO4·5H2O、盐酸、苛性钾、次氯酸、氨气
⑧ 金属元素和非金属元素形成的化合物不一定是离子化合物
A. 3个B. 4个C. 5个D. 6个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全世界每年因钢铁锈蚀造成大量的损失。某城市拟用如图方法保护埋在弱碱性土壤中的钢质管道,使其免受腐蚀。关于此方法,下列说法正确的是( )
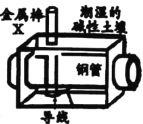
A.钢管附近土壤的pH小于金属棒附近土壤
B.钢管上的电极反应式为:O2+2H2O+4e-=4OH-
C.金属棒X的材料应该是比镁活泼的金属
D.也可以外接直流电源保护钢管,直流电源正极连接金属棒X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以TiO2为催化剂的光热化学循环分解CO2反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如下图所示。
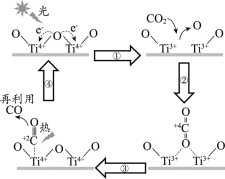
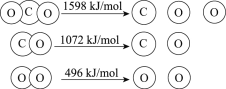
下列说法正确的是
A.过程①中钛氧键断裂会释放能量
B.该反应中,光能和热能转化为化学能
C.使用TiO2作催化剂可以降低反应的焓变,从而提高化学反应速率
D.CO2分解反应的热化学方程式为2CO2(g) =2CO(g) + O2(g) ΔH= + 30 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二硫化钼是重要的固体润滑剂,被誉为“高级固体润滑油之王”。利用低品相的辉钼矿(含MoS2、SiO2以及CuFeS2等杂质)制备高纯二硫化钼的一种生产工艺如图:
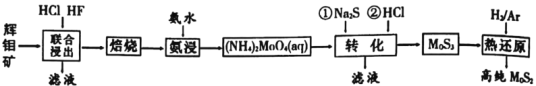
(1)(NH4)2MoO4中Mo的化合价为___。
(2)“焙烧”时MoS2转化为MoO3的化学方程式为___。
(3)“转化”中第一步加入Na2S后,(NH4)2MoO4转化为(NH4)2MoS4,写出第二步(NH4)2MoS4与盐酸生成MoS3的离子方程式为___。
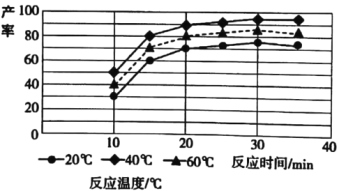
(4)由图分析可知产生MoS3沉淀的流程中选择的最优温度和时间是__,利用化学平衡原理分析低于或高于最优温度时,MoS3的产率均下降的原因___。
(5)利用低品相的原料制备高纯产品是工业生产中的普遍原则。如图所示,反应[Ni(s)+4CO(g)![]() Ni(CO)4(g)] ΔH<0在充满CO的石英管中进行,先在温度为T2的一端放入未提纯的粗镍粉末,一段时间后,在温度为T1的一端得到了纯净的镍粉,请结合平衡移动原理,判断温度Tl___T2(填“>”、“<”或“=”)。
Ni(CO)4(g)] ΔH<0在充满CO的石英管中进行,先在温度为T2的一端放入未提纯的粗镍粉末,一段时间后,在温度为T1的一端得到了纯净的镍粉,请结合平衡移动原理,判断温度Tl___T2(填“>”、“<”或“=”)。

(6)已知Ksp(BaSO4)=1.1×10-10,Ksp(BaMoO4)=4.0×10-8,不纯的Na2MoO4溶液中若含少量可溶性硫酸盐杂质,可加入Ba(OH)2固体除去SO42-(忽略溶液体积变化),则当SO42-完全沉淀时,溶液中c(MoO42-)<___mol/L(保留2位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下反应的化学方程式或离子方程
(1)铝与氧化铁在高温下反应(铝热反应)______________;
(2)医学上,用(胃舒平)氢氧化铝治疗胃酸过多,写出反应的离子方程式____________;
(3)工业上用焦炭和二氧化硅反应制得粗硅(Si)______________;
(4)苯的硝化反应______________;
(5)乙醇和钠反应______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种短周期元素在周期表中的位置如图所示。若X的最高正价与负价的代数和为2,则下列说法不正确是( )
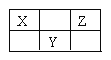
A.最简单气态氢化物稳定性Z>X
B.Z无氧酸溶液能在玻璃容器上刻标记
C.X的氢化物可用作制冷剂
D.原子半径由大到小为Y>Z>X
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com