
1934年,科学家首先从人尿中分离出具有生长素效应的化学物质——吲哚乙酸,吲哚乙酸的结构如右图所示。下列有关吲哚乙酸的说法中正确的是
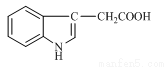
A.吲哚乙酸与苯丙氨酸互为同分异构体
B.吲哚乙酸可以发生取代反应、加成反应、氧化反应和还原反应
C.1 mol吲哚乙酸与足量氢气发生加成反应时,可以消耗5 mol H2
D.吲哚乙酸苯环上的二氯代物共有四种结构
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016学年安徽省高二上学期第三次月考化学试卷(解析版) 题型:选择题
在已经处于化学平衡状态的体系中,如果下列量发生变化,其中一定能表明化学平衡移动的是
A.反应混合物的浓度 B.反应体系的压强 C.正、逆反应的速率 D.反应物的转化率
查看答案和解析>>
科目:高中化学 来源:2016届安徽省皖江名校高三上学期12月联考化学试卷(解析版) 题型:填空题
CCUS是一种二氧化碳的捕获、利用与封存的技术,这种技术可将CO2资源化,产生经济效益.
(1)已知:①CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H1=-820kJ/mol
②CO(g)+H2O(g)=CO2(g)+H2(g) △H2=-41.2kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H3=-566kJ/mol
则反应的CO2(g)+CH4(g) 2CO(g)+2H2(g)的△H=___________。
2CO(g)+2H2(g)的△H=___________。
(2)工业上,可利用太阳能以CO2为原料制取C,其原理如下图所示:
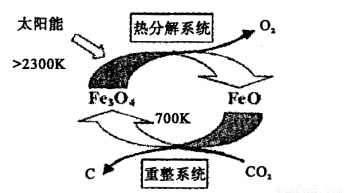
整个过程中__________(填“Fe3O4”或“FeO”)是反应的催化剂。重整系统中发生的反应为6FeO+CO2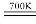 2Fe2O3+C,每生成1molFe3O4,转移电子的物质的量为____________。
2Fe2O3+C,每生成1molFe3O4,转移电子的物质的量为____________。
(3)CO2还可用于合成甲醇,其热化学方程式为:CO2(g)+H2(g) CH3OH(g)+H2O(g) △H<0
CH3OH(g)+H2O(g) △H<0
①该反应的平衡常数表达式为____。
②在恒容的密闭容器中,加入H2和CO2的混合气体,不同温度条件,反应相同时间后,测得甲醇的体积分数甲(CH3OH)如图所示。图中A、B、C、D、E五个点对应的状态中,处于平衡状态的是 _______ (填字母),B点和E点的反应速率大小关系为v(B) v(E)(填“>”、“<”、“=”)。
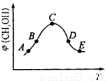
③一定温度下,在甲、乙两个容积相同的密闭容器中,加入H2和CO2的混合气体。
容器 | 甲 | 乙 |
反应物投入量 | 1molCO2、3molH2 | amolCO2、bmolH2、cmolCH3OH(g)、cmolH2O(g) |
甲容器平衡后气体的压强为开始时的80%,要使乙容器达平衡时与甲容器达到相同的平衡状态,且起始时反应逆向进行,则c的取值范围为___________。
查看答案和解析>>
科目:高中化学 来源:2016届河北省张家口市四校高三上学期联考化学试卷(解析版) 题型:选择题
烯烃、一氧化碳和氢气在催化剂作用下生成醛的反应,称为羰基合成,也叫烯烃的醛化反应。由乙烯制丙醛的反应为CH2=CH2+CO+H2  CH3CH2CHO。由分子式为C4H8的烯烃进行醛化反应,得到醛的同分异构体可能有
CH3CH2CHO。由分子式为C4H8的烯烃进行醛化反应,得到醛的同分异构体可能有
A.2种 B.3种
C.4种 D.5种
查看答案和解析>>
科目:高中化学 来源:2016届河北省张家口市四校高三上学期联考化学试卷(解析版) 题型:选择题
下列名称的有机物实际上不可能存在的是
A.2,2-二甲基丁烷 B.2-甲基-4-乙基-1-己烯
C.3-甲基-2-戊烯 D.3,3-二甲基-2-戊烯
查看答案和解析>>
科目:高中化学 来源:2016届湖南省、修水一中高三上学期联考化学试卷(解析版) 题型:选择题
在肉制品加工中,使用护色剂——亚硝酸钠必须严格控制用量,确保食品安全。某一反应体系共有反应物和生成物六种物质:NaNO2、H2O、NO、I2、NaI、HI。已知该反应中NaNO2只发生了如下过程:NaNO2——NO。下列有关说法不正确的是( )
A.氧化剂与还原剂的物质的量之比为1:2
B.若有1mol电子转移,则氧化产物的物质的量是0.5mol
C.据此反应原理,可以在酸性条件下用淀粉碘化钾试纸检验NO2—的存在
D.若误食亚硝酸钠会导致血红蛋白中亚铁离子转化为铁离子而中毒
查看答案和解析>>
科目:高中化学 来源:2016届天津市等六校高三上学期期中联考化学试卷(解析版) 题型:实验题
铁矿石是工业炼铁的主要原料之一,其主要成分为铁的氧化物(设杂质中不含铁元素和氧元素,且杂质不与H2SO4反应)。某研究性学习小组对某铁矿石中铁的氧化物的化学式进行探究。
Ⅰ.铁矿石中含氧量的测定
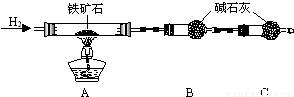
①按如图组装仪器, ;
②将5.0g铁矿石放入硬质玻璃管中,装置B、C中的药品如图所示(夹持仪器均省略);
③从左端导气管口处不断地缓缓通入H2,待C装置出口处H2验纯后,点燃A处酒精灯;
④充分反应后,撤掉酒精灯,再持续通入氢气至完全冷却.
(1)补全步骤①的操作 .
(2)装置C的作用为 .
(3)测得反应后装置B增重1.35g,则铁矿石中氧的质量百分含量为 .
Ⅱ.铁矿石中含铁量的测定

(1)步骤④中煮沸的作用是 .
(2)下列有关步骤⑥的操作中说法正确的是 .
a.因为碘水为黄色,所以滴定过程中不需加指示剂
b.滴定过程中可利用淀粉溶液作为指示剂
c.滴定管用蒸馏水洗涤后可以直接装液
d.锥形瓶不需要用待测液润洗
e.滴定过程中,眼睛注视滴定管中液面变化
f.滴定结束后,30s内溶液不恢复原来的颜色,再读数
(3)若滴定过程中消耗0.5000mol•L﹣1的KI溶液22.50mL,则铁矿石中铁的质量百分含量为 .
Ⅲ.由Ⅰ、Ⅱ可以推算出该铁矿石中铁的氧化物的化学式为 .
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省五校高一上第一次月考化学试卷(解析版) 题型:选择题
用NA表示的值,下列叙述正确的是( )
A.64g SO2含有氧原子数为NA
B.0.5mol/L MgCl2溶液,含有Cl﹣离子数为NA
C.标准状况下,22.4L H2O的分子数为NA
D.常温常压下,14g N2含有分子数为0.5NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高二上学期期中(文)化学试卷(解析版) 题型:选择题
在一个2L的容器内充入6.0mol某气态反应物,经过3s后,它的浓度变成1.2mol/L,在3s内用该反应物浓度的变化表示的反应速率为
A.0.6mol·L—1·s—1 B.0.8mol·L—1·s—1
C.0.4mol·L—1·s—1 D.2.4mol·L—1·s—1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com