
| A.(水晶)SiO2 | B.冰醋酸 | C.氧化镁 | D.白磷 E.固体氩 |
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.可由PH3与HI化合生成 | B.将其加热可以分解 |
| C.能跟NaOH溶液反应 | D.是一种共价化合物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| A.氢键 | B.离子键 | C.共价键 | D.金属键 E.配位键 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氯化钠 | B.二氧化硅 | C.干冰 | D.二氧化硫 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素编号 | 元素特征信息 |
| A | 其单质是密度最小的物质 |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一 |
| C | 其阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物 |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 与C同周期,原子半径在该周期最小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
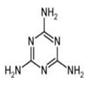
| A.一个分子中共含有15个σ键 |
B.所 有碳原子采用sp2杂化,所有氮原子采用sp3杂化 有碳原子采用sp2杂化,所有氮原子采用sp3杂化 |
| C.属于极性分子,故极易溶于水 |
| D.形成的晶体熔点较高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com