
分析 (1)小苏打与HCl反应生成氯化钠、水和二氧化碳;
(2)逐滴加入Ba(OH)2溶液至中性,生成硫酸钡、硫酸钠和水;
(3)醋酸与碳酸钙反应生成醋酸钙、水和二氧化碳;
(4)反应生成MgO和C;
(5)CO还原氧化铁生成Fe和二氧化碳.
解答 解:(1)小苏打与HCl反应生成氯化钠、水和二氧化碳,离子反应为HCO3-+H+=H2O+CO2↑,故答案为:HCO3-+H+=H2O+CO2↑;
(2)逐滴加入Ba(OH)2溶液至中性,生成硫酸钡、硫酸钠和水,离子反应为2H++SO42-+2OH-+Ba2+=BaSO4↓+2H2O,
故答案为:2H++SO42-+2OH-+Ba2+=BaSO4↓+2H2O;
(3)醋酸与碳酸钙反应生成醋酸钙、水和二氧化碳,离子反应为CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑,
故答案为:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑;
(4)镁条在二氧化碳中剧烈燃烧的反应为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,故答案为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;
(5)高炉炼铁的主要反应为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,故答案为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
点评 本题考查离子反应方程式的书写,为高考常见题型,侧重于学生的分析、应用能力的考查,把握发生的反应及离子反应的书写方法为解答的关键,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 两者相等 | B. | 前者比后者大11倍 | ||
| C. | 后者是前者的108倍 | D. | 后者是前者的1011倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4Cl、HCl、H2O、H2 | B. | Cl2、Na2S、HCl、SO2 | ||
| C. | HBr、CO2、NH3、CS2 | D. | Na2O2、H2O2、H2O、O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
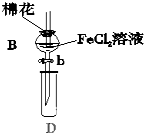 某探究学习小组用如图所示装置进行SO2、Fe2+和Cl-还原性强弱比较实验,实验过程如下:
某探究学习小组用如图所示装置进行SO2、Fe2+和Cl-还原性强弱比较实验,实验过程如下:| 过程Ⅱ中检出离子 | 过程Ⅳ中检出离子 | |
| 甲 | 有Fe3+无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在元素周期表中除短周期外,其他周期均有18种元素 | |
| B. | 只有在原子中,质子数才与核外电子数相等 | |
| C. | 副族元素中没有非金属元素 | |
| D. | 碱金属元素是指IA族的所有元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C(CH3COO-)=C(Cl-)=C(H+)>C(CH3COOH) | B. | C(CH3COO-)=C(Cl-)>C(CH3COH)>C(H+) | ||
| C. | C(CH3COO-)>C(Cl-)>C(H+)>C(CH3COOH) | D. | C(CH3COO-)>C(Cl-)>C( CH3COOH)>C(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 推广使用燃煤脱硫技术,防治SO2污染 | |
| B. | 实施绿化工程,防治扬尘污染 | |
| C. | 研制开发燃料电池汽车,消除机动车尾气污染 | |
| D. | 加大石油、煤炭的开采速度,增加化石燃料的供应量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com