
| A. | $\frac{(a+b)}{4}$ mol/L | B. | 4(3a+b) mol/L | C. | 4(a+b) mol/L | D. | $\frac{(3a+b)}{4}$mol/L |
分析 先根据n=cV分别计算出硫酸铝、硫酸钾的物质的量,再计算出混合液中硫酸根离子的总物质的量,最后根据c=$\frac{n}{V}$计算出稀释后的溶液中SO42-的浓度.
解答 解:500mL a mol/L Al2(SO4)3中含有硫酸铝的物质的量为:amol/L×0.5L=0.5amol,
500mL钾离子浓度为2b mol/L的 K2SO4溶液中含有硫酸钾的物质的量为:2bmol/L×$\frac{1}{2}$×0.5L=0.5bmol,
混合液中含有硫酸根离子的总物质的量为:0.5amol×3+0.5bmol=1.5amol+0.5bmol,
稀释过程中硫酸根离子的物质的量不变,则稀释后的溶液中SO42-的浓度为:$\frac{1.5amol+0.5bmol}{2L}$=$\frac{3a+b}{4}$mol/L,
故选D.
点评 本题考查了物质的量浓度的计算,题目难度中等,明确物质的量浓度的概念及表达式为解答关键,注意溶液稀释过程中溶质的物质的量不变,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 若丙醇中的氧为188O,它与乙酸反应生成的酯的相对分子质量是104 | |
| B. | 用乙酰水杨酸 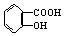 与适量NaOH溶液反应制备 与适量NaOH溶液反应制备 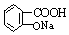 | |
| C. | 向柠檬醛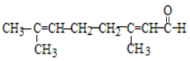 中加入酸性高锰酸钾,若溶液褪色,说明分子中含有醛基 中加入酸性高锰酸钾,若溶液褪色,说明分子中含有醛基 | |
| D. | 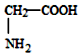 、 、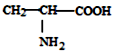 、 、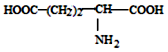 三种氨基酸脱水,最多可生成 6种二肽 三种氨基酸脱水,最多可生成 6种二肽 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含大量SO2的溶液中:NH4+、F-、HCO3-、ClO- | |
| B. | 能使淀粉碘化钾试纸变蓝的溶液:Cl-、Na+、S2-、NH4+ | |
| C. | $\frac{{k}_{w}}{c({H}^{+})}$=10-13mol/L的溶液中:Al3+、Fe3+、NO3-、ClO4- | |
| D. | 滴入KSCN溶液显红色的溶液中:NO3+、Na+、AlO2-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤⑥ | B. | ①②⑤⑥ | C. | ①②③⑤ | D. | ①②③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 肯定有一种元素被氧化,另一种元素被还原 | |
| B. | 在反应中不一定所有元素的化合价都发生变化 | |
| C. | 金属单质在反应中只作还原剂,非金属单质在反应中只作氧化剂 | |
| D. | 金属原子失电子越多,其还原性越强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/min | 0 | 10 | 20 | 30 | 40 |
| n(PCl3)/mol | 4 | 2.8 | 2 | 1 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 编号 | 热化学方程式 | 化学平衡常数 |
| ① | CO(g)+2H2(g)?CH3OH(g)△H1 | K1 |
| ② | 2CH3OH(g)?CH3OCH3(g)+H2O(g)△H2=-24kJ/mol | K2 |
| ③ | CO(g)+H2O(g)?CO2(g)+H2(g)△H3=-41kJ/mol | K3 |
| 化学键 | H-H | C≡O | C-O | H-O | C-H |
| E/(kJ/mol) | 436 | 1076 | 343 | 465 | 413 |
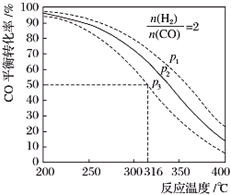
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4:9:24:14:28 | B. | 1:2:5:3:6 | C. | 8:9:12:10:20 | D. | l:l:l:l:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com