
分析 (1)①从海水中提取粗盐,利用海水晒盐,水被蒸发掉;
②重油转变为汽油采用深度裂化的方法;
③利用物质熔沸点不同从石油中提炼汽油、煤油、柴油等;
④煤转化为焦炭、煤焦油等,需要隔绝空气发生复杂的物理、化学变化;
(2)可逆反应达到平衡状态时,正逆反应速率相等,反应体系中各物质的物质的量不变、物质的量浓度不变以及由此引起的一系列物理量不变.
解答 解:(1)①从海水中提取粗盐,利用海水晒盐,水被蒸发掉,属于蒸发原理,故答案为:H;
②重油转变为汽油采用深度裂化即裂解的方法,故答案为:D;
③利用物质熔沸点不同从石油中提炼汽油、煤油、柴油等,属于物理变化,该方法为分馏,故答案为:C;
④煤转化为焦炭、煤焦油等,需要隔绝空气发生复杂的物理、化学变化,为煤的干馏,故答案为:E;
(2)A.N2、H2、NH3的百分含量不再变化时,正逆反应速率相等,反应达到平衡状态,故正确;
B.反应前后气体体积之和减小,当总压强不变时,正逆反应速率相等,反应达到平衡状态,故正确;
C.N2、H2、NH3的分子数之比为1:3:2时,该反应可能达到平衡状态也可能没有达到平衡状态,与反应初始量及转化率有关,所以不能据此判断平衡状态,故错误;
D.N2、H2、NH3的浓度相等时,该反应可能达到平衡状态也可能没有达到平衡状态,与反应初始量及转化率有关,所以不能据此判断平衡状态,故错误;
E.该反应是可逆反应,达到平衡状态时正逆反应速率相等但不停止,故错误;
F.反应速率之比等于其计量数之比且反应方向相反时该反应达到平衡状态,所以v(N2)=v(H2)时一定没有达到平衡状态,故错误;
G.反应前后气体质量不变、容器体积不变,所以密度始终不变,不能根据混合气体的密度判断平衡状态,故错误;
H.混合气体的平均相对分子质量不变时,正逆反应速率相等,反应达到平衡状态,故正确;
I.正反应放出的热量等于逆反应吸收的热量时,正逆反应速率相等,反应达到平衡状态,故正确;
故选:ABHI.
点评 本题考查物质分离和提纯方法的选取及平衡状态判断,为高频考点,明确物质的性质及常见分离提纯方法及平衡状态特点即可解答,注意:只有反应前后改变的物理量才能作为判断依据,不变的物理量不能作为判断依据,如:该题中密度不能作为判断依据,为易错点.


 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案科目:高中化学 来源: 题型:解答题

| 实验一 | 实验二 | |
| 实验药品 | 4g P2O5、8mL无水乙醇 | |
| 实验条件 | 酒精灯加热 | 水浴加热 |
实验现象 | 无水乙醇加入时,圆底烧瓶B中P2O5溶于乙醇,立即产生白雾,当用酒精灯加热后,有气泡产生,并逐渐沸腾,生成粘稠状液体,集气瓶C中有无色液体产生. | 无水乙醇加入时,圆底烧瓶B中P2O5溶于乙醇立即产生白雾,当用水浴加热后,无气泡产生,生成粘稠状液体,集气瓶C中有无色液体产生. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 属于芳香烃 | |
| B. | 能发生取代反应和加聚反应 | |
| C. | 分子式为C15H7O | |
| D. | 不能使溴水褪色但能与氯化铁溶液发生显色反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 | |
| B. | “酸可除锈”、“洗涤剂可去油”都是发生了化学变化 | |
| C. | 煤经气化和液化两个物理变化过程,可变为清洁能源 | |
| D. | 油脂有油和脂肪之分,在酸性条件下水解生成高级脂肪酸和甘油 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过渡元素全部是金属元素 | |
| B. | 元素周期表有18个纵行,即有18个族 | |
| C. | 短周期是指第一、二、三、四周期 | |
| D. | VA族的元素全部是非金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(H2)=0.03 mol/(L•min) | B. | v(N2)=0.02 mol/(L•min) | ||
| C. | v(NH3)=0.01 mol/(L•min) | D. | v(NH3)=0.17 mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铵和碘都可以用加热法进行提纯 | |
| B. | Na、Mg与水反应的溶液中滴入酚酞溶液变红色 | |
| C. | 硫酸亚铁溶液和水玻璃在空气中久置后均会变质 | |
| D. | 氯水和二氧化硫气体均能使品红溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 乙烯的产量可以用来衡量一个国家的石油化工发展水平,这是因为乙烯能够转化为许多重要的有机化工原料,例如:
乙烯的产量可以用来衡量一个国家的石油化工发展水平,这是因为乙烯能够转化为许多重要的有机化工原料,例如: 、
、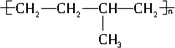 .
. CH3COOC2H5+H2O.
CH3COOC2H5+H2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com