
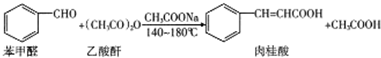
| 名称 | 分子量 | 相对密度 | 熔点 | 沸点 | 溶解度 |
| 苯甲醛 | 106 | 1.04 | -26 | 179.62 | 微溶于水,可混溶于乙醇、乙醚、苯 |
| 乙酸酐 | 102 | 1.080 | -73.1 | 138.6 | 溶于乙醚,易水解形成乙酸. |
| 肉桂酸 | 148 | 1.247 | 135 | 300 | 微溶于水,可以溶于苯、丙酮、乙醚、乙醇等 |
分析 (1)立即加入沸石会引起爆沸;
(2)在蒸馏时用于回流的仪器是球形冷凝管,球形冷凝管能减少反应物的损失;
(3)可逆反应中加入一种反应物过量,能提高另一种反应物的转化率;
(4)NaOH具有碱性,能和酸反应生成钠盐,从而提高酸的溶解性;
(5)NaCl易溶于水,且肉桂酸的溶解度随着温度的降低而减少;从该粗产品中进一步纯化可以采用重结晶的方法;
(6)0.015mol肉桂醛完全反应生成肉桂酸需要0.015mol乙酸酐,实际上乙酸酐的物质的量为0.036mol,则乙酸酐过量,生成的肉桂酸的物质的量为0.015mol,肉桂酸的质量=0.015mol×148g/mol=2.22g,其产率=$\frac{实际质量}{理论质量}×100%$.
解答 解:(1)立即加入沸石会引起爆沸,从而易产生安全事故,所以应该待反应物冷却后补加沸石,
故答案为:待反应物冷却后补加沸石;
(2)在蒸馏时用于回流的仪器是球形冷凝管,球形冷凝管能减少反应物的损失,从而提高反应物的转化率,
故答案为:球形冷凝管;提高反应物转化率;
(3)可逆反应中加入一种反应物过量,能提高另一种反应物的转化率,所以乙酸酐过量的作用是提高苯甲醛的转化率,
故答案为:提高苯甲醛的转化率;
(4)肉桂酸在水中的溶解度较小,肉桂酸具有酸性,能和NaOH反应生成可溶性的钠盐,从而促进肉桂酸的溶解,
故答案为:保证所有的肉桂酸转化为钠盐而溶解;
(5)NaCl易溶于水,肉桂酸不易溶于水,且肉桂酸的溶解度随着温度的降低而减少,所以冰水洗涤的作用是洗去肉桂酸中混有的NaCl,同时降低肉桂酸的溶解度而减少溶解损失;从该粗产品中进一步纯化可以采用重结晶的方法,
故答案为:洗去肉桂酸中混有的NaCl杂质,同时降低肉桂酸的溶解度减少溶解损失;重结晶;
(6)0.015mol肉桂醛完全反应生成肉桂酸需要0.015mol乙酸酐,实际上乙酸酐的物质的量为0.036mol,则乙酸酐过量,生成的肉桂酸的物质的量为0.015mol,肉桂酸的质量=0.015mol×148g/mol=2.22g,其产率=$\frac{实际质量}{理论质量}×100%$=$\frac{1.5g}{2.22g}×100%$=67.6%,
故答案为:67.6%.
点评 本题考查物质制备,为高频考点,涉及实验基本操作、物质分离提纯方法的选取、方程式的有关计算等知识点,侧重考查学生实验操作、实验分析及计算能力,明确实验原理、实验操作及基本计算是解本题关键,注意结合表中信息分析解答,题目难度不大.


科目:高中化学 来源: 题型:选择题
| 化学键 | C-H | C-F. | H-F | F-F |
| 键能/(kJ•mol-1) | 414 | 489 | 565 | 155 |
| A. | -1940kJ•mol-1 | B. | 1940kJ•mol-1 | C. | -485kJ•mol-1 | D. | 485kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热稳定性:HF>H2O>NH3>CH4 | |
| B. | 离子半径:S2->K+>Na+>Al3+ | |
| C. | 碱性:Mg(OH)2<KOH<CsOH | |
| D. | 给出质子的能力:H3PO4<H2SO4<HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应物和生成物都是非极性分子 | |
| B. | 0.5molHCHO 含有1molσ键 | |
| C. | HCHO、CO2分子中中心原子杂化类型相 | |
| D. | 液态水中只存在一种作用力同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用红外光谱来测定有机物分子中不同类型的氢原子和数目 | |
| B. | CH3CH2Br中滴加AgNO3溶液观察是否有浅黄色沉淀,判断卤代烃的类型 | |
| C. | CH3CH2Cl与NaOH的乙醇溶液混合后加热,制得气体通入酸性高锰酸钾溶液中,若溶液褪色,则可检验气体中有乙烯 | |
| D. | 用酸性高锰酸钾溶液区分苯和甲苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol甲基含10NA个电子 | |
| B. | 标准状况下,11.2L三氯甲烷所含的分子数目为0.5NA | |
| C. | 一定条件下,2.6g乙炔、苯和苯乙烯的气态混合物所含碳原子数为0.2NA | |
| D. | 0.5mol聚1,3-丁二烯分子中含有C=C双键数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com