
【题目】下列离子方程式中书写错误的是
A. 氢氧化铜跟稀硫酸反应:Cu(OH)2+2H+![]() Cu2++2H2O B. 碳酸钡跟盐酸反应:BaCO3+2H+
Cu2++2H2O B. 碳酸钡跟盐酸反应:BaCO3+2H+![]() Ba2++H2O+CO2↑
Ba2++H2O+CO2↑
C. 硫化亚铁跟稀硫酸反应:S2-+2H+![]() H2S↑ D. 亚硫酸钠溶液跟稀硫酸反应:SO32-+2H+
H2S↑ D. 亚硫酸钠溶液跟稀硫酸反应:SO32-+2H+![]() H2O+SO2↑
H2O+SO2↑
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列关于能量的变化及反应热的说法中正确的是
A.任何化学反应都有反应热
B.某些化学键断裂时吸收能量,某些化学键断裂时则放出能量
C.形成新化学键不一定放出能量
D.有热量变化的过程一定有化学键的断裂与形成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeSO4受热分解的化学方程式为:2FeSO4![]() Fe2O3+SO2↑+SO3↑
Fe2O3+SO2↑+SO3↑
请回答:
将FeSO4受热产生的气体按图示装置进行实验,证实含有SO2和SO3。能说明SO2存在的实验现象是_______;为测定BaSO4沉淀的质量,后续的操作步骤依次为____、洗涤、干燥、称量。
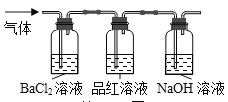
试剂一个实验方案,用化学方法验证FeSO4受热后固体的成分(不考虑其他反应)_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能用离子方程式Ba2++2OH+2H++SO4 2![]() BaSO4↓+2H2O来表示的反应是
BaSO4↓+2H2O来表示的反应是
A. 向硫酸溶液中加入氯化钡溶液
B. 向硫酸溶液中加入氢氧化钡溶液
C. 向氯化钡和氢氧化钠的混合溶液中加入足量硫酸溶液
D. 向氢氧化钡溶液加入少量硫酸和盐酸的混合溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积为VL的恒容密闭容器中盛有一定量H2,通入Br2(g)发生反应:H2(g)+Br2(g)2HBr(g);△H<0. 当温度分别为T1、T2达平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示.下列说法不正确的是( )

A. 由图可知:T1>T2
B. a、b两点的反应速率:b>a
C. 为了提高Br2(g)的转化率,可采取将HBr液化并及时移走的方法
D. T1时,随着Br2(g)加入,平衡时HBr的体积分数不断增加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为2 L的3个密闭容器中发生反应3A(g)+B(g)![]() xC(g),按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:
xC(g),按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:
容器 | 甲 | 乙 | 丙 |
反应物投入量 | 3 mol A、2 mol B | 6 mol A、4 mol B | 2 mol C |
到达平衡的时间/min | 5 | 8 | |
A的浓度/(mol·L-1) | c1 | c2 | |
C的体积分数 | w1 | w3 | |
混合气体密度/(g·L-1) | ρ1 | ρ2 |
下列说法正确的是 ( )
A. 若x<4,则2c1<c2 B. 若w3=w1,可断定x=4
C. 无论x的值是多少,均有2ρ1=ρ2 D. 容器甲中反应从开始到达平衡平均速率为v(A)=0.3 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为实现实验目的,选用的装置、实验操作均正确的是( )
实验目的 | 实验步骤和装置 | |
A | 验证SO2具有漂白性 | 将SO2通入氢氧化钠的酚酞试液中 |
B | 探究温度对反应速率的影响 | 不同温度下,取0.1 mol/LKI 溶液,向其中先加入淀粉溶液,再加入0.1 mol/L 硫酸,记录溶液出现蓝色的时间 |
C | 验证牺牲阳极的阴极保护法 |
往铁电极附近滴加铁氰化钾溶液 |
D | 检验蔗糖水解产物具有还原性 | 向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,再向其中加入新制的Cu(OH)2,加热3-5min。 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将HCl和NaCl分别溶于水。下列说法正确的是( )
A. HCl的离子键被破坏 B. NaCl的共价键被破坏
C. HCl和NaCl的化学键均遭破坏 D. HCl和NaCl的化学键均未遭破坏
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com