
| A、加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,有CO32-或HCO3-中的一种或两种 |
| B、加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
| C、加入硝酸酸化的硝酸银溶液有白色沉淀生成,则溶液中一定含有Cl- |
| D、加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,一定有Ba2+ |


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:
| A、钠在Cl2中燃烧,产生大量黄烟 |
| B、HClO是弱酸,所以NaCIO是弱电解质 |
| C、Cl2通入H2S饱和溶液中出现浑浊,说明氧化性:Cl2>S |
| D、新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
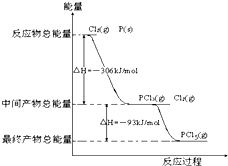 红磷P(s)和Cl2(g)发生反应生成PCl3和PCl5,反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据),根据图回答下列问题:
红磷P(s)和Cl2(g)发生反应生成PCl3和PCl5,反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据),根据图回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、9:1 | B、1:11 |
| C、1:9 | D、11:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
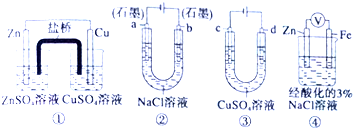
| A、装置①中,盐桥中的K+移向ZnSO4溶液 |
| B、用装置③精炼铜时,c极为粗铜 |
| C、装置②工作一段时间后,a极附近溶液的pH增大 |
| D、装置④中电子Zn流向Fe,装置中有Fe2+生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O2、Na2O均能吸收CO2并放出氧气 |
| B、CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 |
| C、Na比Cu活泼,将Na投入CuSO4溶液中会有铜析出 |
| D、从lL lmol?L-1的H2SO4溶液中取出10 mL,其中H+浓度为2mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件的△H不同 |
| B、相同条件下2mol氢原子所具有的能量小于1 mol氢分子所具有的能量 |
| C、应用盖斯定律,可以计算某些难以直接测量的反应焓变 |
| D、反应NH3(g)+HCl(g)═NH4Cl(s)在室温下可自发进行:则该反应的△H>0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com