
| A. |  | B. |  | C. |  | D. |  |
分析 A、氯化氢为共价化合物,分子中存在一个氢氯共用电子对,氯原子最外层一个为8个电子;
B.二氧化碳分子中存在两个碳氧双键,不是碳氧单键;
C.氢氧根离子中存在一个氧氢键,氧原子最外层为8个电子;
D.次氯酸中存在1个氧氢键和一个氧氯键,不存在氢氯键.
解答 解:A、氯化氢属于共价化合物,分子中存在一个H-Cl键,氯原子最外层达到8个电子,氯化氢正确的电子式为 ,现象中共用电子对不能横写,故A错误;
,现象中共用电子对不能横写,故A错误;
B.二氧化碳分子中的碳氧键为碳氧双键,正确的电子式为: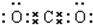 ,故B错误;
,故B错误;
C.氢氧根离子为复杂阴离子,其电子式中需要标出最外层电子数及所带的电荷,氢氧根离子的电子式为: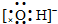 ,故C正确;
,故C正确;
D.次氯酸中不存在氢氯键,次氯酸中存在1个氧氯键和1个氢氧键,次氯酸的电子式为: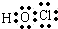 ,故D错误;
,故D错误;
故选C.
点评 本题考查了电子式的书写判断,题目难度中等,注意掌握电子式的概念及正确表示方法,明确离子化合物与共价化合物的电子式的表示方法及区别.


科目:高中化学 来源: 题型:选择题
| A. | 第7周期ⅢA族 | B. | 第7周期ⅤA族 | C. | 第7周期ⅢB族 | D. | 第7周期ⅤB族 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ,B是同周期第一电离能最小的元素,C的最外层有三个单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个单电子,E的外围电子排布式为3d64s2.回答下列问题: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,下列命名正确的是( )
,下列命名正确的是( )| A. | 2,3,4-三甲基己烷 | B. | 2,3-二甲基-4-乙基戊烷 | ||
| C. | 4-乙基-2,3-二甲基戊烷 | D. | 2-乙基-3,4-二甲基戊烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液态氟化氢中有三聚氟化氢(HF)3分子存在 | |
| B. | 冰的密度比液态水的密度小 | |
| C. | H2O的分解温度比H2S高 | |
| D. | 乙醇能与水以任意比混溶而甲醚(CH3-O-CH3)难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在0℃,1.01×105 Pa时,11.2 L氮气所含原子数目为NA | |
| B. | 标准状况下,5.6 L SO3的质量约为20 g | |
| C. | 同温同压下,16 g CH4与44 g CO2具有相同的体积 | |
| D. | 标准状况下,CO和N2的密度相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com