
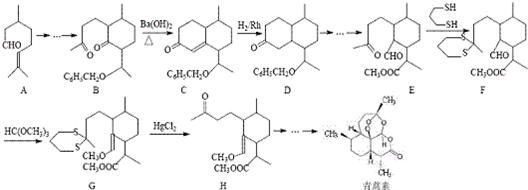
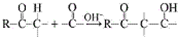
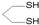
 用系统命名法命名,它的名称是1,3-丙二硫醇;反应B→C,实际上可看作两步进行,依次发生的反应类型是加成反应、消去反应.
用系统命名法命名,它的名称是1,3-丙二硫醇;反应B→C,实际上可看作两步进行,依次发生的反应类型是加成反应、消去反应.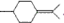 ,则异蒲勒醇的结构简式为:
,则异蒲勒醇的结构简式为: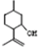 .
. 分析 (1)根据D的结构简式书写分子式,含有的官能团为羰基、醚键;
(2)烃分子中含-OH叫醇,含-SH叫硫醇,物质 用系统命名法命名为1,3-丙二硫醇;
用系统命名法命名为1,3-丙二硫醇;
由题目信息可知,结合B、C的结构可知,C=O双键变成C=C双键,应是B中连接羰基的甲基上的α-H与C=O先发生发生加成反应,再发生消去反应生成C;
(3)A的同系物中相对分子质量最小的分子为CH2=CHCHO,与银氨溶液发生反应生成CH2=CH-COONH4、Ag、NH3与H2O;
(4)由E→F的结构可知,羰基中C=O双键变成C-S单键,由G→H的结构可知C-S单键又变成羰基,目的是保护羰基;
(5)A在Sn-β沸石作用下,可异构为异蒲勒醇,已知异蒲勒醇分子有3个手性碳原子,异蒲勒醇分子内脱水再与一分子H2加成可生成 ,则异蒲勒醇的结构简式为:
,则异蒲勒醇的结构简式为: .
.
解答 解:(1)根据D的结构简式,可知分子式为C20H28O2,含有的官能团为羰基、醚键,
故答案为:C20H28O2;羰基、醚键;
(2)烃分子中含-OH叫醇,含-SH叫硫醇,物质 用系统命名法命名为1,3-丙二硫醇;
用系统命名法命名为1,3-丙二硫醇;
由题目信息可知,结合B、C的结构可知,C=O双键变成C=C双键,应是B中连接羰基的甲基上的α-H与C=O先发生发生加成反应,再发生消去反应生成C,
故答案为:1,3-丙二硫醇;加成反应、消去反应;
(3)A的同系物中相对分子质量最小的分子为CH2=CHCHO,与银氨溶液发生反应生成CH2=CH-COONH4、Ag、NH3与H2O,反应方程式为:CH2=CH-CHO+2Ag(NH3)2OH$\stackrel{△}{→}$CH2=CH-COONH4+2Ag+3NH3+H2O,
故答案为:CH2=CH-CHO+2Ag(NH3)2OH$\stackrel{△}{→}$CH2=CH-COONH4+2Ag+3NH3+H2O;
(4)由E→F的结构可知,羰基中C=O双键变成C-S单键,由G→H的结构可知C-S单键又变成羰基,目的是保护羰基,
故答案为:保护羰基;
(5)A在Sn-β沸石作用下,可异构为异蒲勒醇,已知异蒲勒醇分子有3个手性碳原子,异蒲勒醇分子内脱水再与一分子H2加成可生成 ,则异蒲勒醇的结构简式为:
,则异蒲勒醇的结构简式为: ,
,
故答案为: .
.
点评 本题考查有机物推断与合成,是对有机化学基础的综合考查,侧重考查学生分析推理能力,熟练掌握官能团的性质与转化,难度中等.


科目:高中化学 来源: 题型:解答题
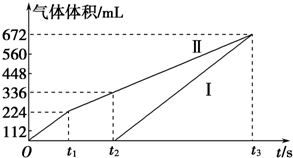
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
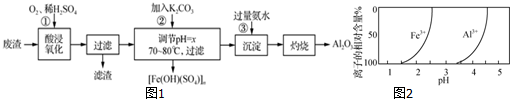
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | X | Y | Z | M | R | Q | |
| 原子半径(×10-10m) | 1.86 | 0.99 | 1.43 | 1.60 | 0.75 | 0.74 | |
| 主要化合价 | 最高正价 | +1 | +7 | +3 | +2 | +5 | -- |
| 最低负价 | -- | -1 | -- | --- | -3 | -2 | |
| A. | 元素X和Q形成的化合物中不可能含有共价键 | |
| B. | X、Z、M的单质分别与水反应,Z最剧烈 | |
| C. | X、Z、R的最高价氧化物对应的水化物之间可两两相互反应 | |
| D. | Y的氧化物对应的水化物的酸性一定强于R的氧化物对应水化物的酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②③ | C. | ③⑤ | D. | ②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
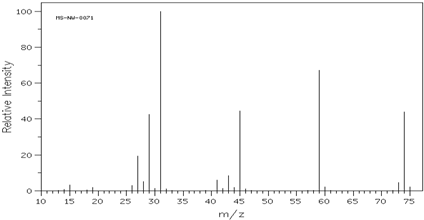
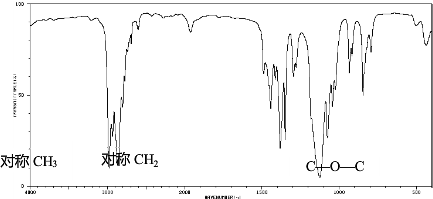
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
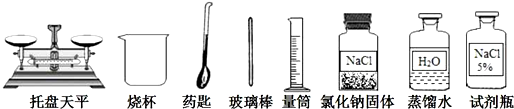
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
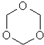 ),三聚甲醛可用作合成工程塑料等,还是日用化妆品冷烫精及脱毛剂的主要原料.下列有关三聚甲醛的说法中正确的是( )
),三聚甲醛可用作合成工程塑料等,还是日用化妆品冷烫精及脱毛剂的主要原料.下列有关三聚甲醛的说法中正确的是( )| A. | 三聚甲醛属于高分子化合物 | |
| B. | 三聚甲醛与甘油互为同分异构体 | |
| C. | 三分子甲醛合成三聚甲醛的反应属于加成反应 | |
| D. | 1 mol的三聚甲醛燃烧时生成CO2和H2O的物质的量一定相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com