
【题目】NH3的催化氧化是工业制取硝酸的关键步骤之一,该反应的化学方程式为:4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g),△H<0。
4NO(g)+6H2O(g),△H<0。
请回答下列问题:
(1)在恒温恒容下判断该反应达到平衡状态的标志是______(填字母)。
a.NH3和NO浓度相等 b.NO百分含量保持不变
c.容器中气体的压强不变 d.NH3的生成速率与NO的消耗速率相等
(2)当该反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高NH3平衡转化率的是_____________。(填字母)
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.降低温度
(3)将0.050 mol NH3 (g)和0.060 mol O2(g)放入容积为1L的密闭容器中,在一定条件下达到平衡,测得c(NO)=0.040 mol/L。计算该条件下反应的NH3的转化率。平衡时,NH3的转化率α(NH3 )=_________。
【答案】bcbd80%
【解析】
(1)a、NH3和NO浓度相等不能说明其浓度保持不变,故无法判断该反应是否达到平衡,故a错误;b、根据化学平衡状态的定义,当组分的百分含量不再变化时反应达到平衡,即NO百分含量不变时反应达到平衡,故b正确;c、反应前后气体系数之和不相等,相同条件下,压强之比等于物质的量之比,即压强不变,说明反应达到平衡,故c正确;d、NH3的生成速率、消耗NO的反应速率,都是向逆反应方向进行,不能说明正反应速率和逆反应速率相等,故无法判断反应是否达到平衡,故d错误;(2)a、再通入N2,恒容状态下,组分的浓度不变,平衡不移动,NH3的转化率不变,故a错误;b、通入O2,增加反应物的浓度,平衡向正反应方向移动,即NH3的转化率增大,故b正确;c、催化剂对化学平衡无影响,NH3的转化率不变,故c错误;d、该反应为放热反应,降低温度,平衡向正反应方向进行,NH3的转化率增大,故d正确;(3)达到平衡时NO的物质的量为0.04×1mol=0.04mol,则消耗NH3的物质的量为0.04mol,即NH3的转化率为0.04/0.05×100%=80%。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
【题目】在常温下,向10mL浓度均为0.1mol·L-1的NaOH和Na2CO3混合溶液中滴0.1mol·L-1的盐酸,溶液pH随盐酸加入体积的变化如图所示。下列说法正确的是

A. 在a点的溶液中,c(Na+)>c(CO32-)>c(Cl-)>c(OH-)>c(H+)
B. 在b点的溶液中,2n(CO32-)+n(HCO3-)<0.001mol
C. 在c点的溶液pH<7,是因为此时HCO3-的电离能力大于其水解能力
D. 若将0.1mol·L-1的盐酸换成同浓度的醋酸,当滴至溶液的pH=7时:c(Na+)=c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究氮氧化物的反应机理,对于消除其对环境的污染有重要意义。
(1)升高温度,绝大多数的化学反应速率增大,但是2NO(g)+O2(g) ![]() 2NO2(g)的反应速率却随着温度的升高而减小。查阅资料知:2NO(g)+O2(g)
2NO2(g)的反应速率却随着温度的升高而减小。查阅资料知:2NO(g)+O2(g) ![]() 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
I.2NO(g) ![]() N2O2(g)(快) △H1<0 v1正=k1正c2(NO) v1逆=k1逆c(N2O2)
N2O2(g)(快) △H1<0 v1正=k1正c2(NO) v1逆=k1逆c(N2O2)
Ⅱ.N2O2(g)+O2(g) ![]() 2NO2(g)(慢) △H2<0 v2正=k2正c(N2O2)c(O2) v2逆=k2逆c2(NO2)
2NO2(g)(慢) △H2<0 v2正=k2正c(N2O2)c(O2) v2逆=k2逆c2(NO2)
请回答下列问题:
①反应2NO(g)+O2(g) ![]() 2NO2(g)的△H=___________(用含△H1和△H2的式子表示)。一定温度下,反应2NO(g)+O2(g)
2NO2(g)的△H=___________(用含△H1和△H2的式子表示)。一定温度下,反应2NO(g)+O2(g)![]() 2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=___________,升高温度,K值___________(填“增大”“减小”或“不变”)
2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=___________,升高温度,K值___________(填“增大”“减小”或“不变”)
②决定2NO(g)+O2(g)![]() 2NO2(g)反应速率的是反应Ⅱ,反应I的活化能E1与反应Ⅱ的活化能E2的大小关系为E1___________E2(填“>”“<”或“=”)。由实验数据得到v2正~c(O2)的关系可用图表示。当x点升高到某一温度时,反应重新达到平衡,则变为相应的点为___________(填字母)。
2NO2(g)反应速率的是反应Ⅱ,反应I的活化能E1与反应Ⅱ的活化能E2的大小关系为E1___________E2(填“>”“<”或“=”)。由实验数据得到v2正~c(O2)的关系可用图表示。当x点升高到某一温度时,反应重新达到平衡,则变为相应的点为___________(填字母)。
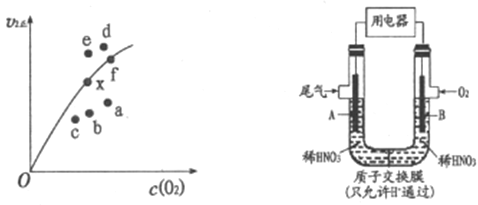
(2)通过图所示装置,可将汽车尾气中的NO、NO2转化为重要的化工原料HNO3,其中A、B为多孔惰性电极。该装置的负极是__________ (填“A”或“B”),B电极的电极反应式为__________。
(3)实验室可用NaOH溶液吸收NO2,反应为2NO2+2NaOH=NaNO3+NaNO2+H2O。含0.2 mol NaOH的水溶液与0.2 mol NO2恰好完全反应得1L溶液甲,溶液乙为0.1mol/L的CH3COONa溶液,则两溶液中c(NO3-)、c (NO2-)和c(CH3COO-)由大到小的顺序为__________(已知HNO2的电离常数Kα=7.1×10-4mol/L,CH3COOH的电离常数Kα=1.7×10-5mol/L)。可使溶液甲和溶液乙的pH相等的方法是__________。
a.向溶液甲中加适量水 b.向溶液甲中加适量NaOH
c.向溶液乙中加适量水 d.向溶液乙中加适量NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】大气污染物氟利昂—12的分子式是CF2Cl2,它是一种卤代烃,关于氟利昂—12的说法错误的是( )
A.它有两种同分异构体
B.化学性质虽稳定,但在紫外线照射下,可发生分解,产生的氯原子可引发损耗 O3的反应
C.大多数无色
D.它可看作甲烷分子的氢原子被氟、氯原子取代后的产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.氯水能导电,所以氯气是电解质
B.碳酸钙不溶于水,所以它是非电解质
C.固体磷酸是电解质,所以磷酸在熔融状态下和溶于水时都能导电
D.胆矾虽不能导电,但它属于电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁可与等物质的量的硫酸铵生成硫酸亚铁铵,析出晶体的化学式为( NH4)2Fe(SO4)2·6H2O。该物质可以溶于水而不溶于乙醇,是一种复盐,在空气中比一般亚铁盐稳定,常被用作氧化还原滴定的基准物。下面是某实验小组制取硫酸亚铁铵的部分装置与实验步骤:
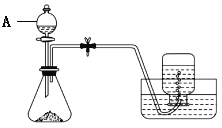
①称取约5 g铁屑放入锥形瓶中,加入15 mL 10% Na2CO3溶液,小火加热10分钟,倒掉剩余的碱液后,用蒸馏水洗净铁屑,干燥。
②称取2.24 g 铁屑放入锥形瓶中,由分液漏斗滴加20 mL 3 mol/L硫酸溶液。
③待反应结束后,由分液漏斗加入适量的(NH4)2SO4溶液,并将上述混合溶液转移至蒸发皿中,缓慢加热,浓缩至表面出现晶膜为止。
④放置冷却,析出晶体,过滤、用无水乙醇洗涤、干燥。
请回答下列问题:
(1)仪器A的名称是___________。
(2)实验开始前,检查反应装置气密性的方法为_______________________________。
(3)步骤①中小火加热的作用是________________________。
(4)步骤②中滴加硫酸溶液时留取少许溶液于分液漏斗中的原因是___________________。
(5)步骤③中理论上需加入2 mol/L (NH4)2SO4溶液______________mL。
(6)无水乙醇洗涤晶体的作用是_______________________________。
(7)取1.00 g高锰酸钾样品,再加入硫酸酸化,并配成250 mL溶液。取出25.00 mL,用浓度为0.1000 mol/L的(NH4)2Fe(SO4)2标准溶液滴定,终点时用去标准液20.00 mL。则滴定时发生反应的离子方程式为_____,该样品中高锰酸钾的质量分数为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛(![]() )抗腐蚀性能好,露置于空气中数年,仍光亮如初.以金红石(主要成分是
)抗腐蚀性能好,露置于空气中数年,仍光亮如初.以金红石(主要成分是![]() )为原料生产金属钦的步骤主要有:①在高温下,向金红石与焦炭的混合物中通入氯气(
)为原料生产金属钦的步骤主要有:①在高温下,向金红石与焦炭的混合物中通入氯气(![]() ),得到
),得到![]() 和一种可燃性气体;②在稀有气体环境和加热条件下,用
和一种可燃性气体;②在稀有气体环境和加热条件下,用![]() 和
和![]() 反应得到
反应得到![]() 和
和![]() ,下列说法不正确的是
,下列说法不正确的是
A. ①中的反应![]()
B. ②中的稀有气体的作用是隔绝空气
C. ②中发生的反应为置换反应
D. 金属钛在常温下不与![]() 反应
反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com