
| A. | ④、③ | B. | ④、② | C. | ①、② | D. | ③、① |
分析 溶质的质量分数=$\frac{{m}_{溶质}}{{m}_{溶液}}$×100%,根据体质数据找出溶质质量、溶液质量,然后带人表达式进行计算即可;注意①胆矾为CuSO4•5H2O,溶于水溶质为硫酸铜;②中氢氧化钙的溶解度较小,5.1g氢氧化钙不会完全溶解.
解答 解:①7.5g胆矾溶于100g水中,胆矾的化学式为CuSO4•5H2O,则7.5g胆矾中含有硫酸铜的质量为:7.5g×$\frac{160}{250}$=4.8g,则该溶液中硫酸铜的质量分数为:$\frac{4.8g}{100g+7.5g}$×100%≈4.5%;
②5.1g Ca(OH)2放入100g水中,常温下氢氧化钙的溶解度为0.16g,则该溶液为饱和溶液,氢氧化钙的质量分数为:$\frac{0.16g}{100g+0.16g}$×100%≈0.16%;
③向50g 8%的NaOH溶液中加入50g水,溶质氢氧化钠的质量为:50g×8%=4g,则加入水后的溶液中氢氧化钠的质量分数为:$\frac{4g}{50g+50g}$×100%=4%;
④已知20℃时KMnO4 的溶解度为6.4g,用100g水,在20℃时配成KMnO4 的饱和溶液中溶质的质量分数为:$\frac{6.4g}{100g+6.4g}×100%$≈6%;
根据分析可知,四种溶液的溶质质量分数最大的为④,溶质质量分数最小为②,
故选B.
点评 本题考查了溶质质量分数的计算,题目难度中等,注意掌握溶质质量分数的表达式及计算方法,①②为易错点,注意①中溶质为硫酸铜、②中氢氧化钙在常温下溶解度约为0.16g.


科目:高中化学 来源: 题型:选择题
| A. | 高纯硅制作光导纤维 | B. | 石墨制作火箭发动机喷管 | ||
| C. | 地沟油水解制取肥皂 | D. | 有机垃圾发酵生产沼气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 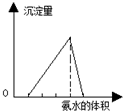 图可表示向酸化的AlCl3溶液中逐滴加入稀氨水,沉淀量与氨水体积的关系 | |
| B. | 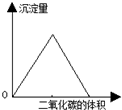 图中可表示向澄清石灰水中通入二氧化碳气体,沉淀量与二氧化碳体积的关系 | |
| C. |  图中可表示向亚硫酸溶液中通入硫化氢,沉淀量与硫化氢气体的关系 | |
| D. | 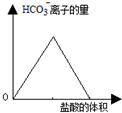 图中可表示向碳酸钠溶液中逐滴加入稀盐酸,HCO3-离子的量与盐酸体积的关系 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1 FeSO4溶液中:K+,NH4+,MnO4-,ClO- | |
| B. | 澄清透明的溶液中:Fe3+,Mg2+,SO42-,Br- | |
| C. | c(H+)=$\sqrt{{K}_{W}}$的溶液中:K+,Al3+,Cl-,SO42- | |
| D. | 使酚酞变红色的溶液:Na+,NH2CH2COOH,I-,Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
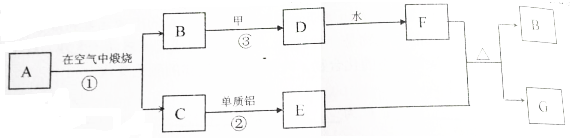
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
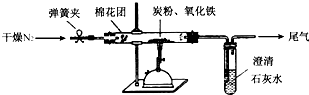
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫化钠水解:S2-+2H2O?H2S+2OH- | |
| B. | 向Ba(OH)2溶液中滴加稀H2SO4:H++OH-═H2O | |
| C. | 向CuCl2溶液中加入H2S溶液:Cu2++S2-═CuS↓ | |
| D. | CaCO3溶于稀HCl:CaCO3+2H+═Ca2++CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{48}^{95}$Cd和${\;}_{48}^{97}$Cd互为同素异形体 | |
| B. | ${\;}_{48}^{95}$Cd和${\;}_{48}^{97}$Cd质量数相同 | |
| C. | ${\;}_{48}^{95}$Cd和${\;}_{48}^{97}$Cd是同一种核素 | |
| D. | ${\;}_{48}^{95}$Cd和${\;}_{48}^{97}$Cd互为同位素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com