
| A. | 该实验不需要指示剂 | |
| B. | 用量筒量取上述硫酸的体积 | |
| C. | H2SO4的浓度为1.00 mol•L-1 | |
| D. | 参加反应的H+和OH-的物质的量相等 |
分析 A.没有指示剂无法判断滴定终点;
B.量筒的精确度太低;
C.根据氢氧化钠的量计算硫酸的浓度;
D.强酸与强碱恰好反应,说明氢离子与氢氧根离子完全反应.
解答 解:A.没有指示剂无法判断滴定终点,所以用NaOH溶液滴定硫酸时要加指示剂,故A错误;
B.量筒的精确度太低,应该用酸式滴定管来量取硫酸的体积,故B错误;
C.20.00mL 0.50mol•L-1NaOH溶液,恰好将未知浓度的H2SO4溶液20.00mL,设硫酸的浓度为cmol/L,则0.50mol•L-1×0.0200L=2c×0.0200L,所以c=0.25mol•L-1,故C错误;
D.强酸与强碱恰好反应,说明氢离子与氢氧根离子完全反应,则参加反应的H+和OH-的物质的量相等,故D正确.
故选D.
点评 本题考查酸碱中和滴定,把握酸碱滴定实验中指示剂的选择、反应终点为解答的关键,侧重分析与实验能力的考查,注意中和热判断,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
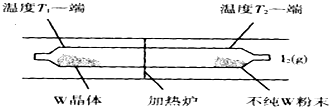
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
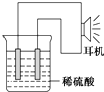 乙同学利用生活中常见的物品,根据氧化还原反应知识和电化学知识,自己动手设计一个原电池.请填写下列空白:
乙同学利用生活中常见的物品,根据氧化还原反应知识和电化学知识,自己动手设计一个原电池.请填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:选择题

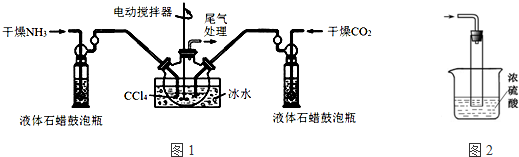
| A. | 酸碱中和反应是放热反应 | |
| B. | 图1所示的反应为吸热反应 | |
| C. | 图2装置中铜片是负极,锌片表面有气泡出现 | |
| D. | 图2装置是将电能转变为化学能的装置 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
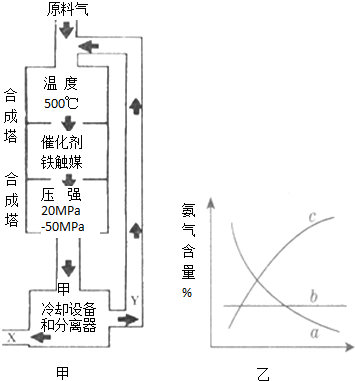 利用所学化学知识解答问题:
利用所学化学知识解答问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
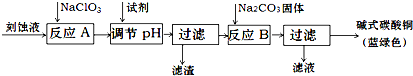
| 物质 | Cu(OH)2 | Fe (OH)2 | Fe (OH)3 |
| 开始沉淀pH | 4.2 | 5.8 | 1.2 |
| 完全沉淀pH | 6.7 | 8.3 | 3.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能自发进行 | B. | 不能自发进行 | ||
| C. | 可能自发进行 | D. | 在加热条件下才能自发进行 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com