
| A. | 可以电解熔融的氯化钠来制取金属钠 | |
| B. | 可以将钠加入氯化镁饱和溶液中制取镁 | |
| C. | 用电解法冶炼铝时,原料是氯化铝 | |
| D. | 在浓缩的海水加入新制氯水即可得到液溴 |
分析 金属冶炼的方法主要有:
热分解法:对于不活泼金属,可以直接用加热分解的方法将金属从其化合物中还原出来(Hg及后边金属);
热还原法:在金属活动性顺序表中处于中间位置的金属,通常是用还原剂(C、CO、H2、活泼金属等)将金属从其化合物中还原出来(Zn~Cu);
电解法:活泼金属较难用还原剂还原,通常采用电解熔融的金属化合物的方法冶炼活泼金属(K~Al);
浓缩的海水加氯水得到溴水.
解答 解:A.钠是活泼金属,可以用电解熔融的氯化钠的方法来制取金属钠,故A正确;
B.钠是很活泼金属,将Na加入氯化镁溶液中,Na先和水反应生成NaOH,NaOH再和氯化镁发生复分解反应,所以得不到Mg单质,可以采用电解熔融氯化镁的方法冶炼Mg,故B错误;
C.电解冶炼铝时,原料是氧化铝,因为氯化铝是分子晶体,熔融状态下氯化铝不导电,故C错误;
D.浓缩的海水加氯水得到溴水,此时得到的溴水的浓度较小,得不到液溴,故D错误;
故选A.
点评 本题考查了金属的冶炼,根据金属活动性强弱确定冶炼方法,易错选项是C,注意冶炼金属铝的原料不是氯化铝而使氧化铝,且需要加冰晶石降低其熔点,题目难度不大.


科目:高中化学 来源: 题型:选择题
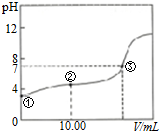
| A. | 两溶液反应的离子方程式是H++OH-+H2O | |
| B. | 图中②点所示溶液中:2c(Na+)=c(HA)+c(A-) | |
| C. | 图中②点所示溶液中:c(A-)>c(H+)>c(HA)>c(OH-) | |
| D. | 图中③点所示滴入的NaOH溶液的体积V=20.00mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 检验自来水中含有Cl- | B. | 检验鸡蛋壳中含有碳酸盐 | ||
| C. | 检验加碘食盐中加的不是碘单质 | D. | 除去热水瓶中的水垢 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子直径的大小 | B. | 分子数目的多少 | ||
| C. | 组成分子的原子个数 | D. | 分子间距离的大小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碱金属单质的密度都比水小 | |
| B. | 碱金属单质都是还原剂 | |
| C. | 碱金属单质的熔沸点一般随着原子的电子层数的增多而升高 | |
| D. | 碱金属单质在氧气中燃烧,产物都是过氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3 NaHCO3 NaOH Na2O2 | B. | NaOH Na2O2 Na2CO3 NaHCO3 | ||
| C. | NaHCO3 Na2CO3 NaOH Na2O2 | D. | NaHCO3 Na2CO3 Ca(OH)2 CaCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁与稀盐酸反应 2Fe+6H+═2Fe3++3H2↑ | |
| B. | 硝酸银溶液中加入铜粉 Ag++Cu═Cu2++Ag | |
| C. | 氧化铜与盐酸反应 O2-+2H+═H2O | |
| D. | 碳酸镁跟稀硫酸反应:MgCO3+2H+═Mg2++H2O+CO2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com