
下列离子方程式书写正确的是()
A. 向碳酸钠溶液中滴加与其溶质的物质的量相等的盐酸:CO32﹣+2H+=CO2↑+H2O
B. Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3﹣+Ca2++OH﹣=CaCO3↓+H2O
C. 足量铁粉与稀硝酸反应:Fe+4H++NO3﹣=Fe3++2H2O+NO↑
D. 向漂白粉溶液中通入少量二氧化硫:Ca2++2ClO﹣+SO2+H2O=CaSO3↓+2HClO
考点: 离子方程式的书写.
专题: 离子反应专题.
分析: A.反应生成碳酸氢钠和氯化钠;
B.Ca(HCO3)2溶液与少量NaOH溶液反应生成碳酸钙沉淀和水;
C.足量铁粉与稀硝酸反应生成Fe2+;
D.向漂白粉溶液中通入少量二氧化硫,发生氧化还原反应生成硫酸钙和氯化钙.
解答: 解:A.向碳酸钠溶液中滴加与其溶质的物质的量相等的盐酸:CO32﹣+H+=HCO3﹣,故A错误;
B.Ca(HCO3)2溶液与少量NaOH溶液反应生成碳酸钙沉淀和水,离子方程式为HCO3﹣+Ca2++OH﹣=CaCO3↓+H2O,故B正确;
C.足量铁粉与稀硝酸反应生成Fe2+,离子方程式为3Fe+8H++2NO3﹣=3Fe2++4H2O+2NO↑,故C错误;
D.向漂白粉溶液中通入少量二氧化硫,发生氧化还原反应生成硫酸钙和氯化钙,离子方程式为SO2+Ca2++ClO﹣+H2O=CaSO4↓+2H++Cl﹣,故D错误.
故选B.
点评: 本题考查离子反应方程式书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重与量有关的离子反应、氧化还原反应的离子反应考查,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
氮化硅是一种高温陶瓷材料,它硬度大、熔点高,化学性质稳定,工业上普遍采用高纯硅与纯氮在1 300 ℃反应获得。
(1)根据性质,推测氮化硅陶瓷的用途是________。(填序号)
A.制汽轮机 B.制有色玻璃
C.制永久性模具 D.制造柴油机
(2)写出N的原子结构示意图__________,根据元素周期律知识,请写出氮化硅的化学式_______________________________________________________。
(3)氮化硅陶瓷抗腐蚀能力强,除氢氟酸外,它不与其他无机酸反应,试推测该陶瓷被氢氟酸腐蚀的化学方程式___________________________________。
(4)现用四氯化硅与氮气在氢气气氛保护下,加强热发生反应,可得较高纯度的氮化硅,反应的化学方程式为_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式中,属于水解反应的是( )
|
| A. | HCO3﹣+H2O⇌H3O++CO32﹣ | B. | HCO3﹣+H2O⇌H2CO3+OH﹣ |
|
| C. | CO2+H2O⇌HCO3﹣+H+ | D. | CH3COOH⇌CH3COO﹣+H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)下列实验操作或对实验事实的叙述中不正确的是 (填序号)
①乙醇中含有少量水可加入生石灰再蒸馏制得无水乙醇
②配制银氨溶液时,将硝酸银慢慢滴入稀氨水溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止
③制乙烯时,温度计应插入反应混合液中并控制温度在170℃
④向苯酚溶液中加入少量的稀溴水有白色沉淀生成
⑤实验室制备乙酸乙酯时吸收液为氢氧化钠溶液
⑥检验C2H5Cl中氯元素时,将C2H5Cl与NaOH水溶液混合加热,然后加入AgNO3溶液,观察是否有白色沉淀生成.
(2)现有下列8种有机物:(填选项,否则不得分)
A.甲苯 B苯乙烯 C苯酚 D溴乙烷 E乙醇 F甲醛 G乙酸 H甲酸钠
①能与氢气发生加成反应的有 .
②能发生消去反应的有 .
③能与氢氧化钠溶液反应的有 .
④常温下能与溴水发生取代反应的有 .
⑤能与乙酸发生酯化反应的有 .
⑥能与FeCl3溶液反应,并使溶液呈紫色的有 .
⑦能发生银镜反应的有 .
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值.下列说法正确的是()
A. 25℃时,pH=13的氨水中含有OH﹣的数目为0.1NA
B. 标准状况下,2.24 LNO2 与水反应生成NO3﹣的数目为0.1NA
C. 1 mol Na被完全氧化生成Na2O2,转移电子的数目为NA
D. 4.0 g H2与足量O2完全反应生成水,反应中断裂共价键的总数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是()
A. 一定温度下,在固定体积的密闭容器中发生可逆反应A(s)+B(g)═C(g)+D(g),当混合气体的密度不再改变时,说明已达到化学平衡状态
B. 对于反应C(s)+CO2(g)═2CO(g)△H>0,改变某一条件,若化学平衡常数增大,则反应速率也一定增大
C. 常温下向0.1mol•L﹣1的NH3•H2O中加入氯化铵固体,则溶液中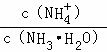 减小
减小
D. 常温下向Mg(OH)2悬浊液中加入MgCl2浓溶液后,溶液中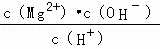 不变
不变
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F、X存在如图甲所示转换关系,其中,A是一种正盐,B是气态氢化物,C是单质,F是强酸.X可能是强酸,也可能是强碱.
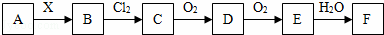
(1)A的化学式是 .
(2)若X是强酸,将D与Cl2同时通入水中发生反应的离子方程式为 .
(3)若X是强碱,过量的B跟Cl2反应除生成C外,另一产物是氯化物.
①过量的B跟Cl2反应的化学方程式为 .
②工业生产中B→D的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
白黎芦醇 广泛存在于食物(如桑椹、花生、尤其是葡萄)中,它可能具有抗癌作用.1mol该物质和Br2、H2分别反应,消耗Br2、H2的物质的量最多为()
广泛存在于食物(如桑椹、花生、尤其是葡萄)中,它可能具有抗癌作用.1mol该物质和Br2、H2分别反应,消耗Br2、H2的物质的量最多为()
A. 1 mol,1 mol B. 3.5 mol,7 mol
C. 3.5 mol,6 mol D. 6 mol,7 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组对奥运会金牌成分提出猜想:甲认为金牌是由纯金制成;乙认为金牌是由金银合金制成;丙认为金牌是由黄铜(铜锌合金)制成。为了验证他们的猜想,请你选择一种试剂来证明甲、乙、丙猜想的正误 ( )。
A.硫酸铜溶液 B.稀硝酸
C.盐酸 D.硝酸银溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com