
【题目】对于可逆反应2AB3(g)![]() A2(g)+3B2(g) △H>0下列图像不正确的是( )
A2(g)+3B2(g) △H>0下列图像不正确的是( )
A.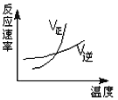 B.
B.
C. D.
D.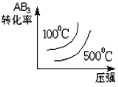
【答案】D
【解析】
可逆反应2AB3(g)A2(g)+3B2(g)△H>0,升高温度,反应速率加快,缩短到达平衡的时间,平衡向正反应方向移动,正反应速率增大的更多,反应物的含量减少;正反应为体积增大的反应,增大压强,平衡逆向移动,反应物的含量增大,以此来解答。
A. 2AB3(g)![]() A2(g)+3B2(g) △H>0升高温度,反应速率加快;因为正反应吸热,升高温度,平衡正向移动,故不选A;
A2(g)+3B2(g) △H>0升高温度,反应速率加快;因为正反应吸热,升高温度,平衡正向移动,故不选A;
B.温度越高,化学反应速率越快,到达平衡所需时间越短;由于正反应吸热,温度升高,有利于反应正向进行,剩余反应物百分含量减少,故不选B;
C.升高温度,平衡正向进行,平衡后AB3的百分含量越低;正反应为体积增大的反应,增大压强,平衡逆向移动,反应物的含量增大,故不选C;
D.正反应为体积增大的反应,增大压强,平衡逆向移动,反应物的转化率应该减小;正反应为吸热反应,当压强相同时,温度越高,越有利于反应正向移动,反应物转化率越高,故选D;
答案:D


科目:高中化学 来源: 题型:
【题目】海藻中含有丰富的碘元素。如图是实验室从海藻里提取碘的流程的一部分。下列判断正确的是

A. 步骤④的操作是过滤
B. 可用淀粉溶液检验步骤②的反应是否进行完全
C. 步骤①、③的操作分别是过滤、萃取
D. 步骤③中加入的有机溶剂可能是酒精或四氯化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组以链烧烃 (C4H6) 和丙烯醛( CH2= CHCHO) 为原料合成某药物中间体环戊基甲酸(部分反应条件、产物已省略),其流程如下:
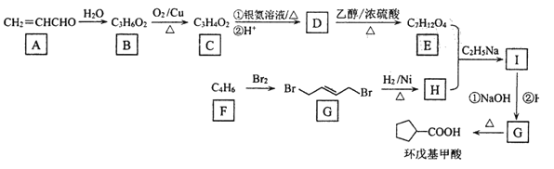
已知:i.![]() +2RBr
+2RBr 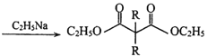 +2HBr
+2HBr
ii. ![]() +2CO2
+2CO2
请回答下列问题:
(1) B中的官能团名称为________,D→E的反应类型是 ____________ .
(2)写出C与银氨溶液反应的化学方程式①:_____________ 。
(3)一定条件下,H可制取F, 则所需试剂和反应条件是____________________ 。
(4) I的结构简式为______________。
(5)环戊基甲酸与苯酚反应生成一种酯X,写出一种同时符合以下条件的 X 的同分异构体的结构简式:________(不考虑立体异构)。
①核磁共振氢谱有四组峰,峰面积比为9:2:2:l
②能与FeCl3发生显色反应
③与浓溴水反应时,l molX可消耗4mol Br2
(6)参照上述合成路线,设计以乙醇和化合物E为原料制备2.2-二乙基丙二酸(结构简式: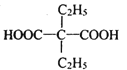 )的合成路线(无机试剂任选):___________________。
)的合成路线(无机试剂任选):___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列三个反应:
①Cl2+FeI2=FeCl2+I2
②2Fe2++Br2=2Fe3++2Br-
③Co2O3+6HCl=2CoCl2+Cl2↑+3H2O
下列说法正确的是( )
A. 反应①②③中的氧化产物分别是I2、Fe3+、CoCl2
B. 根据以上方程式可以得到氧化性:Cl2>Fe3+>Co2O3
C. 在反应③中当1 mol Co2O3参加反应时,2 mol HCl被氧化
D. 可以推理得到Cl2+FeBr2 =FeCl2+Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2.8 g CO和0.2 g H2在足量的氧气中充分燃烧,使生成的CO2和水蒸气通过过量的过氧化钠,完全反应后固体的质量变化量是( )
A. 增加了3.0 gB. 减少了3.0 gC. 增加了2.6 gD. 减少了2.6 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】治理大气和水体污染对建设美丽家乡,打造宜居环境具有重要意义。
(1)![]() 泄漏会导致人体中毒,用于检测
泄漏会导致人体中毒,用于检测![]() 的传感器的工作原理如图所示:
的传感器的工作原理如图所示:

①写出电极Ⅰ上发生的反应式:__________
②工作一段时间后溶液中![]() 的浓度__________(填“变大”、“变小”或“不变”)
的浓度__________(填“变大”、“变小”或“不变”)
(2)用![]() 氧化
氧化![]() 制取
制取![]() ,可提高效益,减少污染。反应为:
,可提高效益,减少污染。反应为:![]() ,通过控制条件,分两步循环进行,可使
,通过控制条件,分两步循环进行,可使![]() 转化率接近100%,其原理如图所示:
转化率接近100%,其原理如图所示:

过程Ⅰ的反应为:![]()
过程Ⅱ反应的热化学方程式(![]() 用含有
用含有![]() 和
和![]() 的代数式表示)__________。
的代数式表示)__________。
(3)在温度![]() ,容积为
,容积为![]() 的绝热容器中,充入
的绝热容器中,充入![]() ,发生反应:
,发生反应:![]() ,容器中
,容器中![]() 的相关量随时间变化如图所示。
的相关量随时间变化如图所示。

①反应到![]() 时,
时,![]() 的转化率是__________。
的转化率是__________。
②根据图示,以下各点表示反应达到平衡状态的是________。
a.![]() b.
b.![]() c.
c.![]() d.
d.![]()
③![]() 内容器中
内容器中![]() 的反应速率增大,而
的反应速率增大,而![]() 后容器中
后容器中![]() 的反应速率减小了,原因是_______。
的反应速率减小了,原因是_______。
④此容器中反应达平衡时,温度若为![]() ,此温度下的平衡常数
,此温度下的平衡常数![]() =__________。
=__________。
(4)工业上可用![]() 溶液吸收法处理
溶液吸收法处理![]() ,25℃时用
,25℃时用![]() 的
的![]() 溶液吸收
溶液吸收![]() ,当溶液
,当溶液![]() 时,溶液中各离子浓度的大小关系为:
时,溶液中各离子浓度的大小关系为:![]() 。(已知25℃时:
。(已知25℃时:![]() 的电离常数
的电离常数![]() ,
,![]() )请结合所学理论通过计算说明
)请结合所学理论通过计算说明![]() 的原因__________。
的原因__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KMnO4在医疗上有广泛地应用,可用于防腐、制药、消毒等。现以软锰矿(主要成分为MnO2,含有少量Al2O3、SiO2等)为原料制备KMnO4的工业流程如图所示。

(1)料渣的主要成分是____,操作2的意义是__________。
(2)“调pH”的目的是__________;写出“氧化”过程中发生反应的离子方程式:________;熔融过程中,氧化剂与还原剂的物质的量之比为_______。
(3)操作3的内容为蒸发浓缩、趁热过滤、洗涤、烘干,已知KHCO3、KMnO4的溶解度曲线是下图中的两种,则KHCO3、KMnO4的溶解度曲线分别是_____(填序号)。

(4)用惰性电极电解K2MnO4溶液也可得到目标产物,则生成目标产物的电极反应式为___________,充分电解后,得到的溶液中溶质的主要成分是______和KMnO4。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国某物理研究所取得重大科技成果,研制出由18O所构成的单质气体。18O是一种稳定的同位素,称为重氧。下列有关说法不正确的是( )
A.1.8 g 18O构成的双原子气体分子的物质的量是0.05 mol
B.0.1 mol重氧水H218O所含的中子数约为6.02×1023
C.0.2 mol 18O2气体的体积约为4.48 L
D.18O2的摩尔质量为36 g·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氢氧化铝Al(OH)3是一种治疗胃酸(含盐酸)过多的药物,用化学方程式表示该反应的原理.___________________________________________
(2)NaHCO3是制作糕点的常用疏松剂,写出NaHCO3受热分解的化学方程式
___________________________________
(3)取少量Fe2O3粉末(红棕色)加入适量盐酸,该反应的离子方程式为______________________;用此溶液进行以下反应,取少量溶液于一支试管中,滴入NaOH溶液,可观察到有红褐色沉淀生成,反应的离子方程式为____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com