
| A£® | 2ÖÖ | B£® | 3ÖÖ | C£® | 4ÖÖ | D£® | 5ÖÖ |
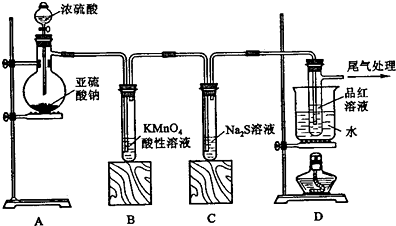
·ÖĪö ¶žŃõ»ÆĮņ¼ČÓŠŃõ»ÆŠŌÓÖÓŠ»¹ŌŠŌ£¬¶ų¶žŃõ»ÆĢ¼ŌŚČÜŅŗÖŠ²»·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬ŌņĄūÓƶžŃõ»ÆĮņµÄ»¹ŌŠŌ¼°Ęư׊ŌĄ“Ēų·ÖSO2ŗĶCO2ĘųĢ壬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗ¢ŁSO2ŗĶCO2¶¼ŹōÓŚĖįŠŌŃõ»ÆĪļ£¬ĖüĆĒ¶¼ÄÜŹ¹Ba£ØOH£©2ČÜŅŗ±ä»ė×Ē£¬²»Äܼų±š£¬¹Ź“ķĪó£»
¢Ś¶žŃõ»ÆĮņÓėĖįŠŌBa©vNO3©w2ČÜŅŗ·¢ÉśŃõ»Æ»¹Ō·“Ӧɜ³ÉĮņĖįøĘ³Įµķ£¬¶ų¶žŃõ»ÆĢ¼²»·“Ó¦£¬ĻÖĻó²»Ķ¬£¬æɼų±š£¬¹ŹÕżČ·£»
¢ŪSO2Ņ²¾ßÓŠ»¹ŌŠŌ£¬Äܱ»KMnO4ĖįŠŌČÜŅŗŃõ»Æ£ØČÜŅŗĶŹÉ«£©£¬¶ųCO2ƻӊ“ĖŠŌÖŹ£¬ĖłŅŌÄÜĄūÓĆKMnO4ĖįŠŌČÜŅŗĒų±šSO2ŗĶCO2£¬¹ŹÕżČ·£»
¢ÜSO2»¹¾ßÓŠĘư׊Ō£¬ÄÜŹ¹Ę·ŗģČÜŅŗĶŹÉ«£¬¶ųCO2ƻӊ“ĖŠŌÖŹ£¬ĖłŅŌÄÜĄūÓĆĘ·ŗģČÜŅŗĒų±šSO2ŗĶCO2£¬¹ŹÕżČ·£»
¢Ż¶žŃõ»ÆĢ¼”¢¶žŃõ»ÆĮņ¶¼æÉŹ¹Na2SiO3ČÜŅŗ±ä»ė×Ē£¬²»Äܼų±š£¬¹Ź“ķĪó£»
¢Ž¶žŃõ»ÆĢ¼ÓėNaHCO3ČÜŅŗ²»·“Ó¦£¬¶žŃõ»ÆĮņæÉÉś³É¶žŃõ»ÆĢ¼ĘųĢ壬µ«¶¼“ÓČÜŅŗÖŠŅŻ³öĘųĢ壬²»Äܼų±š£¬¹Ź“ķĪó£¬
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹµÄ¼ų±š£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕĪļÖŹµÄŠŌÖŹ¼°ŠŌÖŹµÄ²īŅģĪŖ½ā“šµÄ¹Ų¼ü£¬×¢Ņā¶žŃõ»ÆĮņµÄĘư׊Ō¼°·¢ÉśµÄŃõ»Æ»¹Ō·“Ó¦£¬ĢāÄæÄŃ¶Č²»“ó£®


 ÓÅŅķŠ”°ļŹÖĶ¬²½æŚĖćĻµĮŠ“š°ø
ÓÅŅķŠ”°ļŹÖĶ¬²½æŚĖćĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀČ“¦ĄķŅūÓĆĖ®Ź±£¬ŌŚĻļ¾µÄɱ¾śŠ§¹ū±ČŌŚ¶¬¼¾ŗĆ | |
| B£® | ĘųĻó»·¾³±ØøęÖŠŠĀŌöµÄ”°PM2.5”±ŹĒ¶ŌŅ»ÖÖŠĀ·Ö×ÓµÄĆčŹö | |
| C£® | ½«Ė®°ÓµÄøÖĢśÕ¢ĆÅÓėÖ±Į÷µēµÄøŗ¼«ĻąĮ¬æÉŅŌ·ĄÕ¢ĆÅøÆŹ“ | |
| D£® | ĆŗµÄøÉĮóæÉŅŌµĆµ½±½”¢¼×±½µČĢž£¬²»ÄܵƵ½ŃÜÉśĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ¢ńA | ¢ņA | ¢óA | ¢ōA | ¢õA | ¢öA | ¢÷A | 0 | ||
| 2 | ¢Ł | ¢Ś | ¢Ū | ||||||
| 3 | ¢Ü | ¢Ż | ¢Ž | ¢ß | ¢ą | ||||
| 4 | ¢į | ¢ā |
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ±ūČ© | B£® | ±ūĻ©Č© | C£® | ¼×Č© | D£® | ¶”Ļ©Č© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ņõ¼«£ŗ2H++2e-=H2”ü””””””””””””Ńō¼«£ŗ4OH--4e-=2H2O+O2”ü | |
| B£® | Ņõ¼«£ŗCu2++2e-=Cu””””””””””””””Ńō¼«£ŗ4OH--4e-=2H2O+O2”ü | |
| C£® | Ņõ¼«£ŗ2H++2e-=H2”ü””””””””””””Ńō¼«£ŗ2Cl--2e-=Cl2”ü | |
| D£® | Ņõ¼«£ŗCu2++2e-=Cu””””””””””””””Ńō¼«£ŗ2Cl--2e-=Cl2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | CH4”¢C2H4”¢C3H4 | |
| B£® | CH4”¢C3H8”¢C2H2£ØC2H8”¢C2H2ĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ3£© | |
| C£® | C2H6”¢C4H6”¢C2H2£ØĪļÖŹµÄĮæÖ®±ČĪŖ2£ŗ1£ŗ2£© | |
| D£® | C3H8”¢C4H8”¢C2H2£ØÖŹĮæÖ®±ČĪŖ11£ŗ14£ŗ26£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ×ŖŅĘŹ±Ć»ÓŠĻ“µÓ2”«3“Ī | |
| B£® | ¶ØČŻŹ±£¬ø©ŹÓŅŗĆęŹ¹Ö®ÓėæĢ¶ČĻßĻąĘ½ | |
| C£® | ČܽāŹ±·Å³öĮĖ“óĮæµÄČČ£¬µ«Ī“µČĪĀ¶Č»Öø“ĪŖ³£ĪĀ¾ĶæŖŹ¼×ŖŅĘ | |
| D£® | ×ŖŅĘČÜŅŗĒ°£¬ČŻĮæĘæ²»øÉŌļ£¬ĮōĻĀÉŁĮæµÄĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com