
| A. | ①②③ | B. | ③④ | C. | ②⑤⑥ | D. | ①②④⑤⑥ |
分析 ①量筒量取5mL蒸馏水应该选用10mL量筒;
②称量没有腐蚀性固体药品时,不能把药品放在托盘上称量,应该垫上质量相同的纸片;
③浓硫酸沾到皮肤上应该先用抹布擦拭,不能直接用水冲洗;
④应该将试剂瓶口与容器口紧靠在一起;
⑤取块状固体一般用镊子取用;
⑥广口瓶用来保存固体,细口瓶保存液体.
解答 解:①用50mL量筒量取5mL蒸馏水,误差太大,应该用10mL量筒,故①错误;
②应在托盘上各放一张质量相同的纸片,以免污染药品,损坏托盘,故②错误;
③浓硫酸沾到皮肤上,要迅速用抹布擦拭,然后用水冲洗,故③错误;
④倾倒液体时,应使试剂瓶口与容器口紧靠在一起,避免液体流到容器外,故④错误;
⑤固体药品取用时,取用粉末状固体用药匙,块状固体一般用镊子,故⑤错误;
⑥药品保存时,细口瓶保存细口瓶盛液体,广口瓶才用来保存固体,故⑥错误;
故选D.
点评 本题考查化学实验方案的评价,涉及计量仪器的使用方法、药品的取用及保存方法、化学实验安全及事故处理等知识,题目难度不大,要求学生熟练掌握常用仪器的使用方法、药品的正确取用和保存方法,试题培养了学生的化学实验能力.


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:实验题
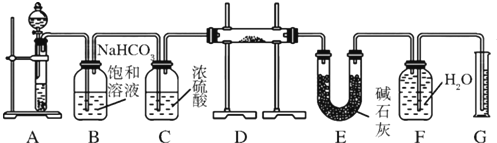
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
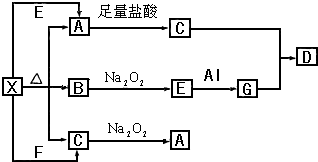
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向NaAlO2溶液中通入少量CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- | |
| B. | Fe3O4溶解在过量的稀硝酸中:Fe3O4+8H+═Fe2++2Fe3++4H2O | |
| C. | 向AlCl3溶液中加入过量的NH3•H2O:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 用铜除去CuCl2 溶液中少量的FeCl3:Fe2++Cu═Fe3++Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9g水和0.75mol一氧化碳 | B. | 10g氢气和10g氧气 | ||
| C. | 22.4mL氢气(标况)和0.1mol氮气 | D. | 22g二氧化碳和16.8L溴单质(Br2) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,其中氮的化合价为-2.
,其中氮的化合价为-2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 因为SO2有漂白性,所以它能使品红溶液、溴水褪色 | |
| B. | 能使品红溶液褪色的气体不一定是SO2 | |
| C. | SO2、HClO、活性炭都能使红墨水褪色,其原理相同 | |
| D. | SO2和Cl2都有漂白作用,将两种气体同时作用于湿润的有色布条,漂白效果更好 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com